1 乙烯 一.乙烯 1
分子结构 一、乙烯1
分子结构 分子式:C2H4 分子式:C2H 4结构式:H HH C=C H结构简式:CH 2 = CH 2或H 2C = CH 2CH2CH2电子式:H H
H:C::C:H 分子式:C2H4结构式:H HH C=C H结构简式:CH 2 = CH 2或H2C = CH 2CH2CH2电子式:H H
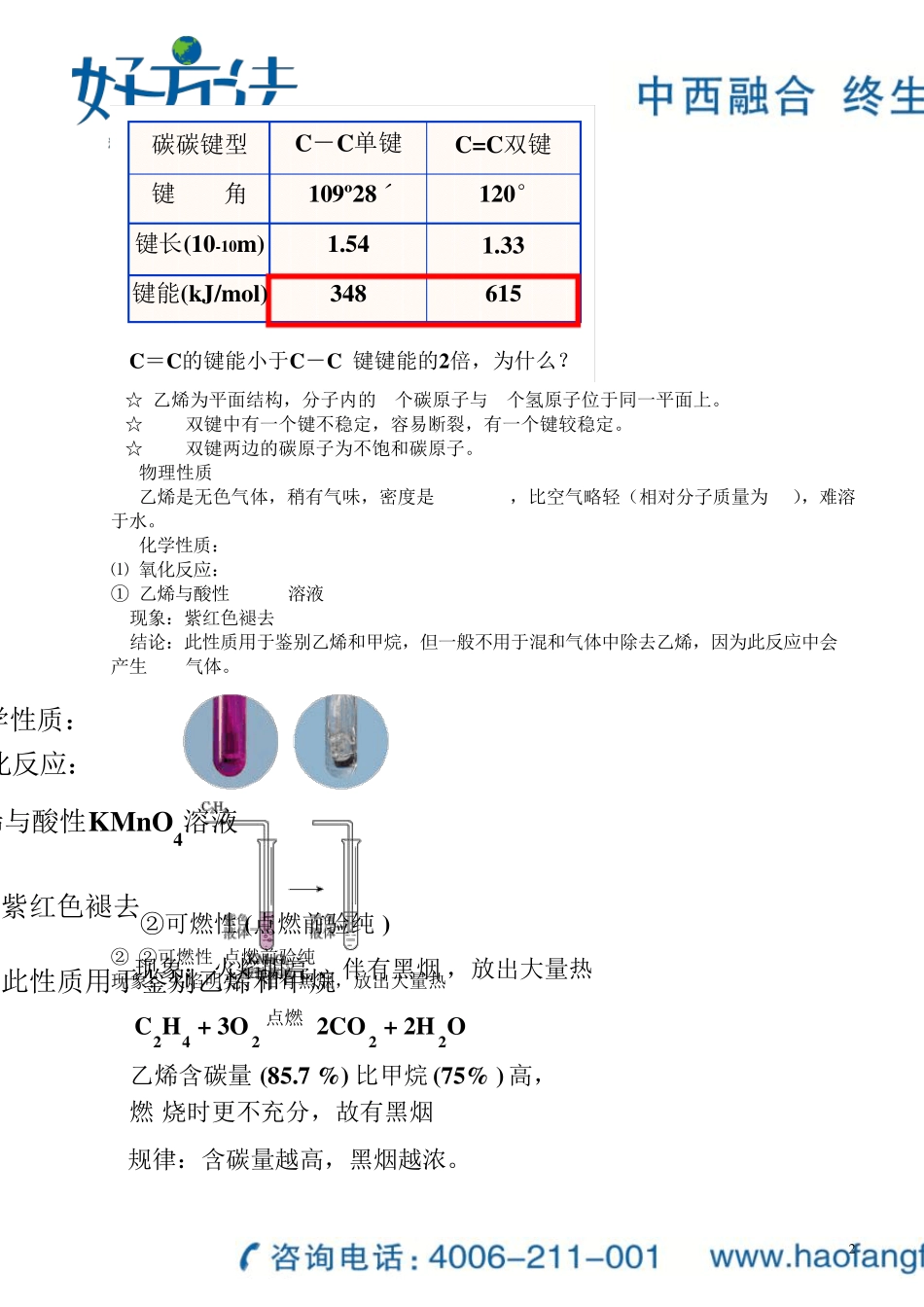
H:C::C:H 平面结构:6个原子共平面,键角120°空间构型 : 乙烷与乙烯的比较结构简式结构式电子式分子式乙烯乙烷C2H6C2H4H:C::C:H::HHH:C:C:H: :: :H HH HH-C-C-H----H HH HH-C = C-H--HHCH3-CH3CH2= CH2 2 615348键能(kJ/mol)1
54键长(10-10m)120°109º28ˊ键角C=C双键C-C单键碳碳键型C=C的键能小于C-C 键键能的2倍,为什么
☆ 乙烯为平面结构,分子内的2个碳原子与4个氢原子位于同一平面上
☆ C=C双键中有一个键不稳定,容易断裂,有一个键较稳定
☆ C=C双键两边的碳原子为不饱和碳原子
物理性质 乙烯是无色气体,稍有气味,密度是1
25 g/L,比空气略轻(相对分子质量为28),难溶于水
化学性质: ⑴ 氧化反应: ① 乙烯与酸性KMnO4溶液 现象:紫红色褪去 结论:此性质用于鉴别乙烯和甲烷,但一般不用于混和气体中除去乙烯,因为此反应中会产生 CO2气体
学性质:化反应:烯与酸性KMnO4溶液:紫红色褪去:此性质用于鉴别乙烯和甲烷 ② ②可燃性(点燃前验纯) 现象:火焰明亮、伴有黑烟,放出大量热 现象: 火焰明亮 、伴有黑烟 ,放出大量热规律:含碳量越高,黑烟越浓
C2H4 + 3O22CO2 + 2H2O点燃②可燃性 (点燃前验纯 )乙烯含碳量 (85