第四章分子结构与反应活性间的定量关系前面我们讨论了分子结构和化学性能之间的关系,如电子效应、溶剂效应和空间效应
但是上述讨论只限于定性
这一章节将分子结构及其反应活性联系起来,建立一方面能够解释反应机理,预测反应速度和平衡的有关关系式
在这里重点介绍哈米特方程式(hammett)
§4-1哈米特方程式一、哈米特方程式的建立37,38年L
Hammett分别在美国和英国化学会志上发表了一系列羧酸酯的水解反应速度常数k与相应羧酸在水中的离解常数Ka的关系
RCOOC2H5+OH-kRCOO-+C2H5OHRCOOH+H2OKaRCOO-+H3O+以lgk为纵坐标,lgKa为横坐标作图,发现间位和对位取代的苯甲酸衍生物有良好的线性关系
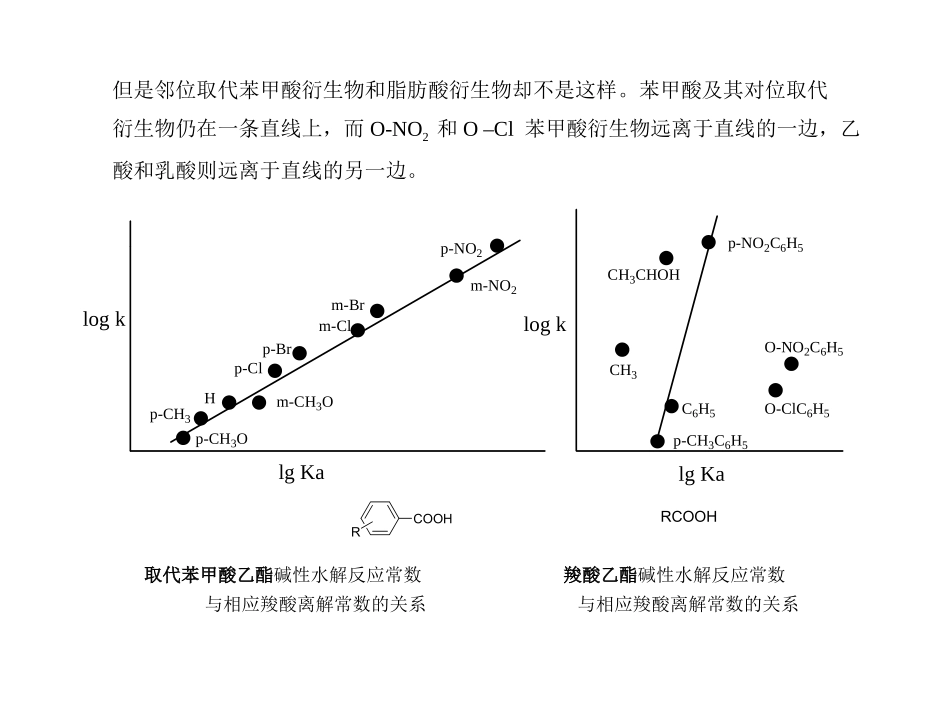
但是邻位取代苯甲酸衍生物和脂肪酸衍生物却不是这样
苯甲酸及其对位取代衍生物仍在一条直线上,而O-NO2和O–Cl苯甲酸衍生物远离于直线的一边,乙酸和乳酸则远离于直线的另一边
p-CH3Op-CH3m-CH3Op-Clp-Brm-Brm-Clm-NO2p-NO2HlgKalogklogklgKap-NO2C6H5p-CH3C6H5CH3CHOHCH3C6H5O-NO2C6H5O-ClC6H5取代苯甲酸乙酯碱性水解反应常数与相应羧酸离解常数的关系羧酸乙酯碱性水解反应常数与相应羧酸离解常数的关系COOHRRCOOH解释:决定化合物化学性质的因素有两种:一是电子效应;二是空间效应
有时其中一个效应占优势,有时另一种效应占优势
有时两者协同作用,有时两者起相反作用
邻位:邻位取代苯甲酸衍生物偏离直线的原因主要是空间效应
间位和对位:由于远离反应中心,不能产生空间效应,因此影响它们水解的主要因素是电子效应
哈米特经过反复的实践,推出了有名的哈米特方程
lgk=lgKa+c(y=bX+c)是一个直线方程,其中为直线的斜率,c为直线的截距,两者都是常数