第十单元 酸和碱一、酸和碱一、酸和碱 HCl H+ + Cl-NaOH Na+ + OH- Ca(OH)2 Ca2+ + 2OH-HNO3 H+ +NO3-H2SO4 2H+ +SO42- KOH K+ + OH- 酸 酸 HH++ + + 酸根离子酸根离子在水溶液中在水溶液中电 离电 离碱 金属离子 碱 金属离子 + + OHOH——在水溶液中在水溶液中电 离电 离二、酸的化学性质1 :酸能与指示剂反应
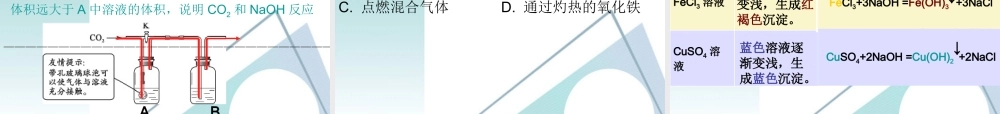
二、酸的化学性质1 :酸能与指示剂反应
遇酸溶液变红色 , 遇碱溶液变蓝色紫色石蕊溶液无色酚酞溶液酸溶液变红色不变色中性溶液不变色不变色碱溶液变蓝色溶液变红色2008-36
部分根据下图所示水、二氧化碳和氧气的性质实验,请回答以下问题
( 2 )将白色纸花用紫色石蕊试液喷湿,放入集气瓶 B 中,观察到的现象是 ___________
纸花由紫色变为红色 二、酸的化学性质2 :酸能与多种活泼金属反应,生成盐和氢气与稀盐酸反应 与稀硫酸反应 镁锌铁Mg + 2HCl = MgCl2 + H2↑ Zn + 2HCl = ZnCl2 + H2↑ Mg + H2SO4 = MgSO4 +H2↑ Zn + H2SO4 = ZnSO4 + H2↑ Fe + 2HCl = FeCl2 + H2↑ Fe + H2SO4 = FeSO4 + H2↑ 注意:金属活动性在 H 以前二、酸的化学性质3 :酸能与某些金属氧化物反应,生成盐和水
现象化学方程式 铁锈+盐酸 铁锈+硫酸 氧化铜 + 盐酸氧化铜 + 硫酸Fe2O3 + 6HCl = 2FeCl3 + 3H2OFe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O CuO + 2HCl = CuCl2 + H2OCuO + H2SO4 = CuSO4 + H2O 溶液由无色逐渐变成黄色,红色固体逐渐消失
溶液由无色逐渐变