1 第十五章 氧族元素之教案 15-1 氧族元素的通性 一:氧族元素通性的变化规律(C级掌握) 1
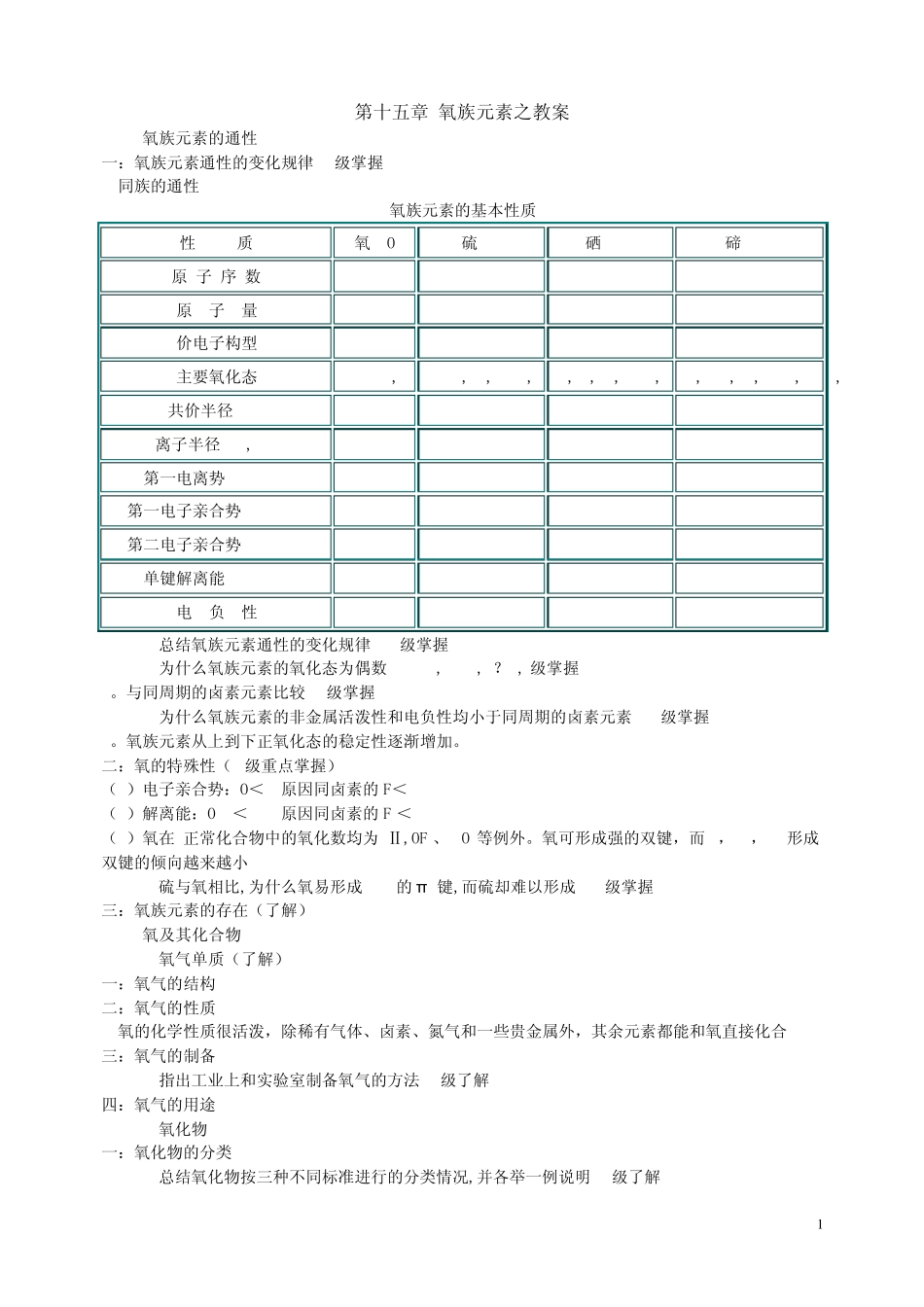
同族的通性 氧族元素的基本性质 性 质 氧(O) 硫(S) 硒(Se) 碲(Te) 原 子 序 数 8 16 34 52 原 子 量 16
96 127
60 价电子构型 2s22p4 3s23p4 4s24p4 5s25p4 主要氧化态 -2,0 -2,0,+2,+4,+6 -2,0,+2,+4,+6 -2,0,+2,+4,+6 共价半径(pm) 66 104 117 137 离子半径(M2-,pm) 140 184 198 221 第一电离势(kJ/mol) 1314 1000 941 869 第一电子亲合势(kJ/mol) -141 -200 -195 -190 第二电子亲合势(kJ/mol) 780 590 420 295 单键解离能(kJ/mol) 142 226 172 126 电 负 性 3
10 15-1
1:总结氧族元素通性的变化规律
(C级掌握) 15-1
2:为什么氧族元素的氧化态为偶数(-2,+2,+4,+6)
(B级掌握) 2
与同周期的卤素元素比较(C级掌握) 15-1
3:为什么氧族元素的非金属活泼性和电负性均小于同周期的卤素元素
(C级掌握) 3
氧族元素从上到下正氧化态的稳定性逐渐增加
二:氧的特殊性(C级重点掌握) (1)电子亲合势:O<S(原因同卤素的F<Cl) (2)解离能:O-0<S-S(原因同卤素的F2<Cl2) (3)氧在 正常化合物中的氧化数均为-Ⅱ,OF2、H2O2等例外
氧可形成强的双键,而 S,Se,Te形成双键的倾向越来越小
4:硫与氧相比,为什么氧易形成 p-p的π 键,而硫却难以形成
(B级掌握) 三:氧族元素的存在(了解) 15-2 氧及其化合物