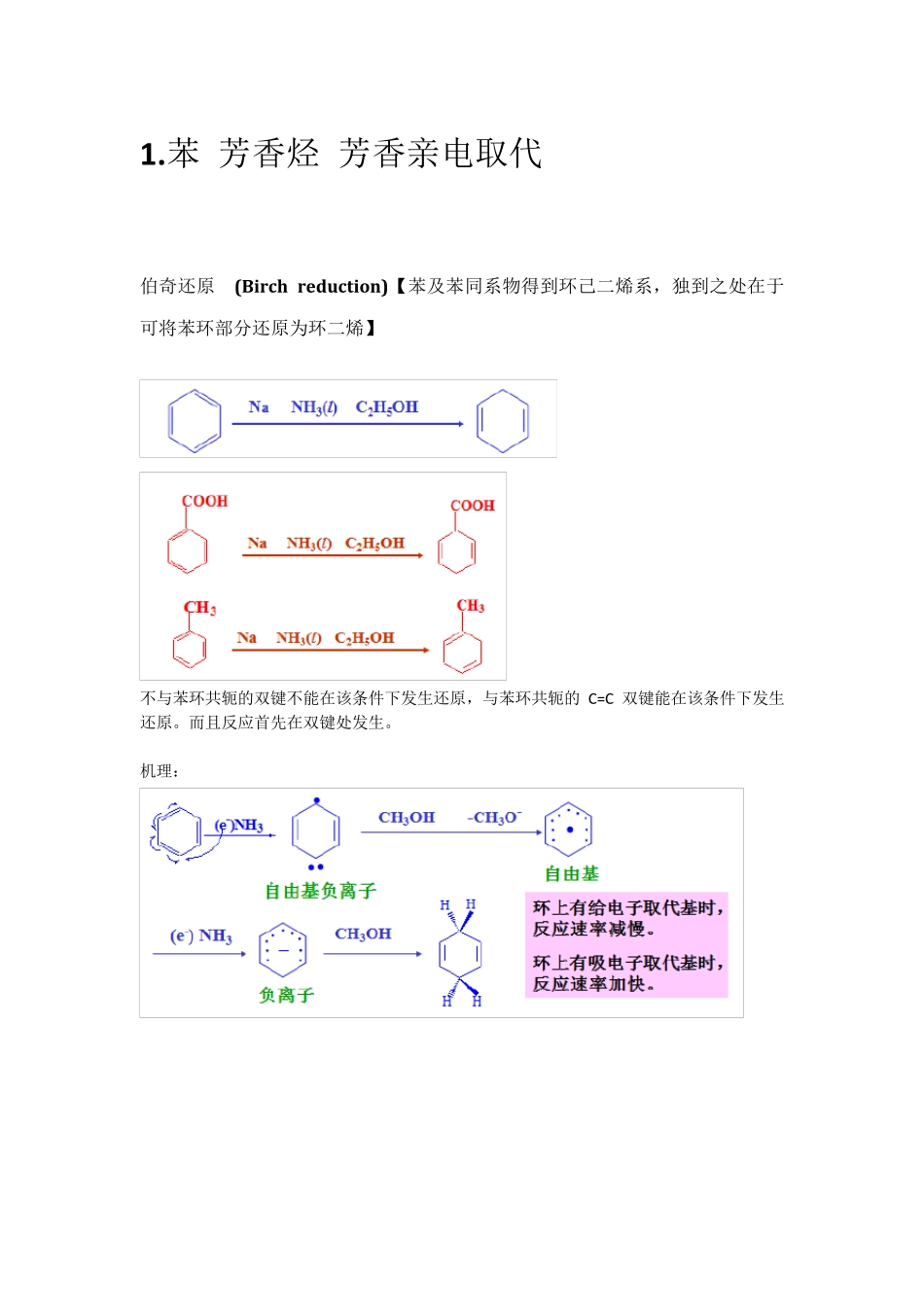
苯 芳香烃 芳香亲电取代 伯奇还原 (Birch redu ction)【苯及苯同系物得到环己二烯系,独到之处在于可将苯环部分还原为环二烯】 不与苯环共轭的双键不能在该条件下发生还原,与苯环共轭的C=C 双键能在该条件下发生还原
而且反应首先在双键处发生
机理: 傅-克(Friedel-Crafts)烷基化反应【苯环上引入烷基】 机理: 特点一:烷基化反应易发生重排,不适合制备长的直链烷基苯
特点二:反应不易控制在一元取代阶段,常常得到一元、二元、多元取代产物的混合物
特点三:反应是可逆的,所以经常发生烷基移位、移环
傅-克(Friedel-Crafts)酰基化反应【苯环上引入酰基,可用于制备芳酮,配合Clemmensen 还原制备直链烷烃】 特点一:酰基是一个钝化的间位定位基,所以反应能控制在一元取代阶段,产率很好
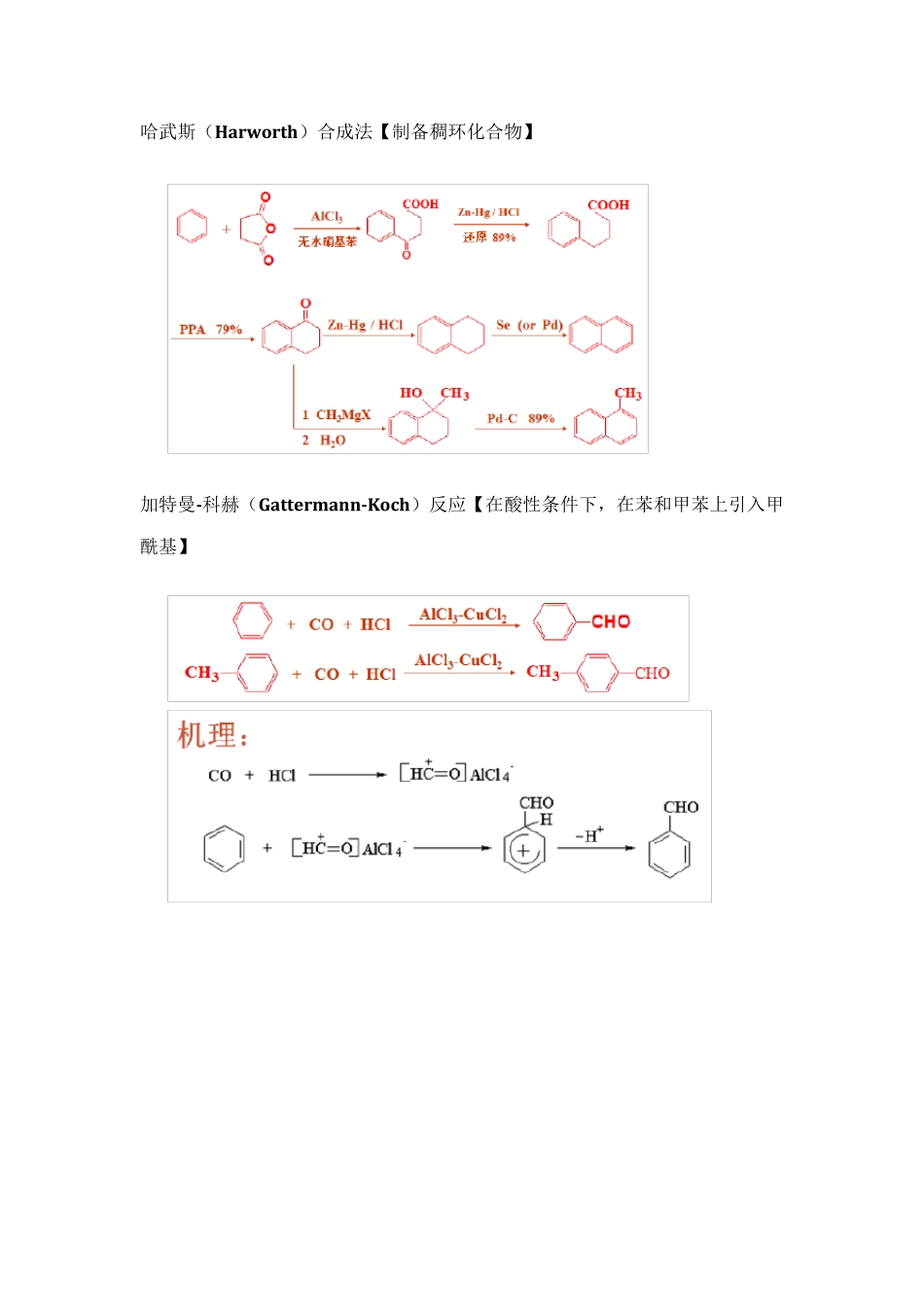
特点二:反应是不可逆的,不会发生取代基的转移反应 哈武斯(Harw orth)合成法【制备稠环化合物】 加特曼-科赫(Gattermann-Koch)反应【在酸性条件下,在苯和甲苯上引入甲酰基】 2
醛、酮 亲核加成 共轭加成 贝克曼(Beckmann)重排【酸性条件下,酮肟转变为酰胺,可用于由酮制备酰胺、羧酸、胺】 (1)重排反应是在酸催化下完成的
(2)只有处于羟基反位的烃基才能迁移
(3)基团的迁移和羟基离去是同步的
(4)迁移基团在迁移过程中构型保持不变
*麦克尔(Michael)共轭加成反应【在碱性催化剂作用下,能提供亲核碳负离子的化合物(给体) 与能提供亲电共轭体系(受体)的化合物发生亲核1,4-共轭加成得到1,5-二羰基化合物】 不对称酮进行麦克尔加成时,反应总是在多取代的α-C 上发生
克莱门森(Clemmensen)还原【酸性条件下将羰基还原成亚甲基】 乌尔夫-凯惜纳-黄鸣龙(Wolffl-Kishner-Huang