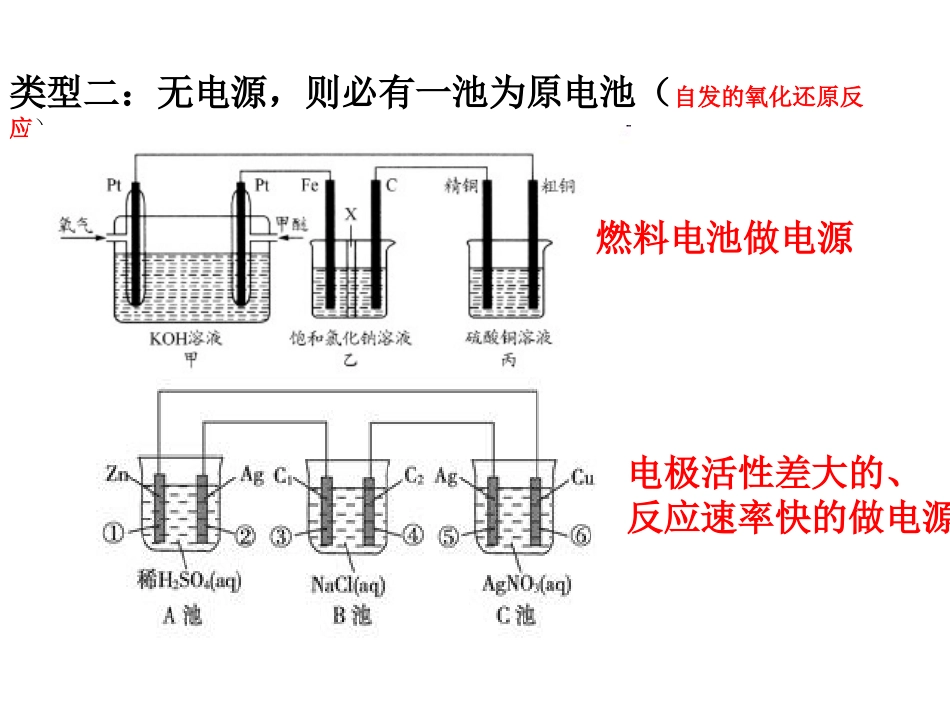
多池串联装置多池串联中必有一个为电解池:类型一:有电源时,各池均为电解池类型二:无电源,则必有一池为原电池(自发的氧化还原反应)燃料电池做电源电极活性差大的、反应速率快的做电源注意:1、阳极的电极材料2、多池串联时,阴、阳极交替出现3、根据阴阳离子的定向移动方向、电极现象等确定电极4、串联电路中电流强度处处相等,根据各极板上得失电子守恒计算议:1
结合基础感知内容总结分析反应装置类型及电极名称的方法
如图X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色色斑向d端扩散
(1)分析电极名称
(2)烧杯中溶液的pH的变化
(3)烧杯中SO42—的移动方向
(4)若去掉X,各电极的的名称,烧杯中的现象
1、结合右图说出装置、电极名称2、若均通入1L甲烷、则转移电子的个数
3、总结判断电极的方法
4、该装置中离子交换膜只允许离子通过
反应一段时间后,向烧杯中加入0
1molCu(OH)2后恰好恢复到反应前的CuSO4溶液的浓度和pH
则反应过程中消耗锌的质量为__________g,烧杯左侧碳棒上析出物质的量为mol
在此过程中烧杯中右侧电极上发生的电极反应方程式为:________________
确定电极名称↓3
利用原电池和电解池原理解题串联电路审题思路1
自发氧化还原反应2
有盐桥的原电池3
二次电池铅蓄电池等常见的原电池产生O21
阳极生氧卤淀粉KI变蓝石蕊变红电极质量减小产生H22
阴极氢金属析出金属PH变大酚酞变红电极判断4e-~4OH-~4H+~2H2~O2~2Cu~2Cl2~4Ag思路;电池中各处电子均相等关系式应用浓差电池1
整理①多池串联装置突破口②电极的判断③关系式的应用2
提问判断正负极:①电解淀粉KI溶液时变蓝的是极;②电解滴加酚酞的NaCl溶液时变红的是极;③通电时F