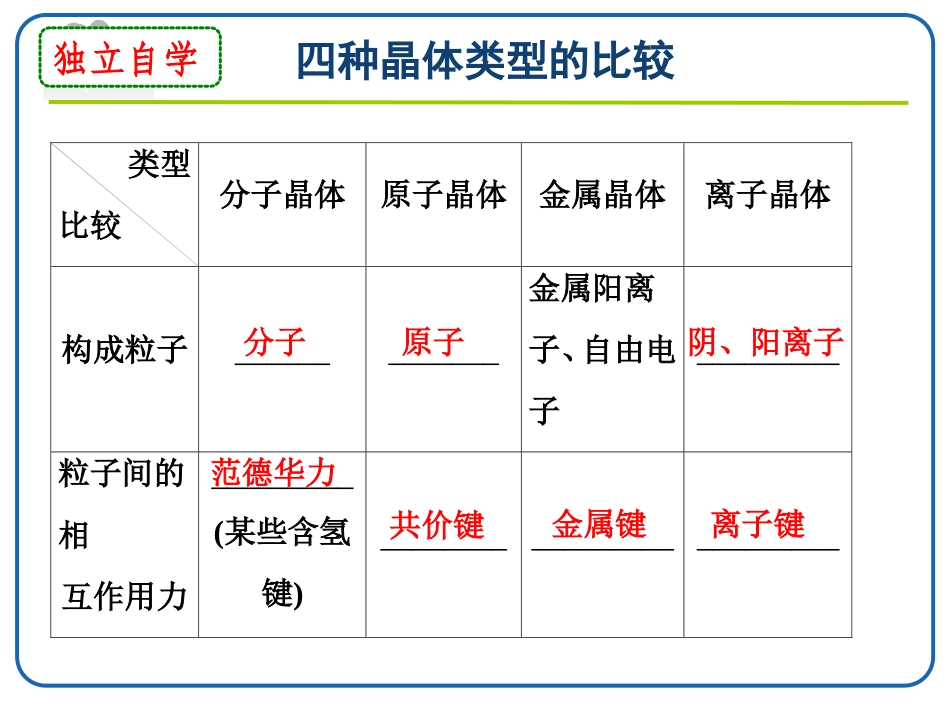
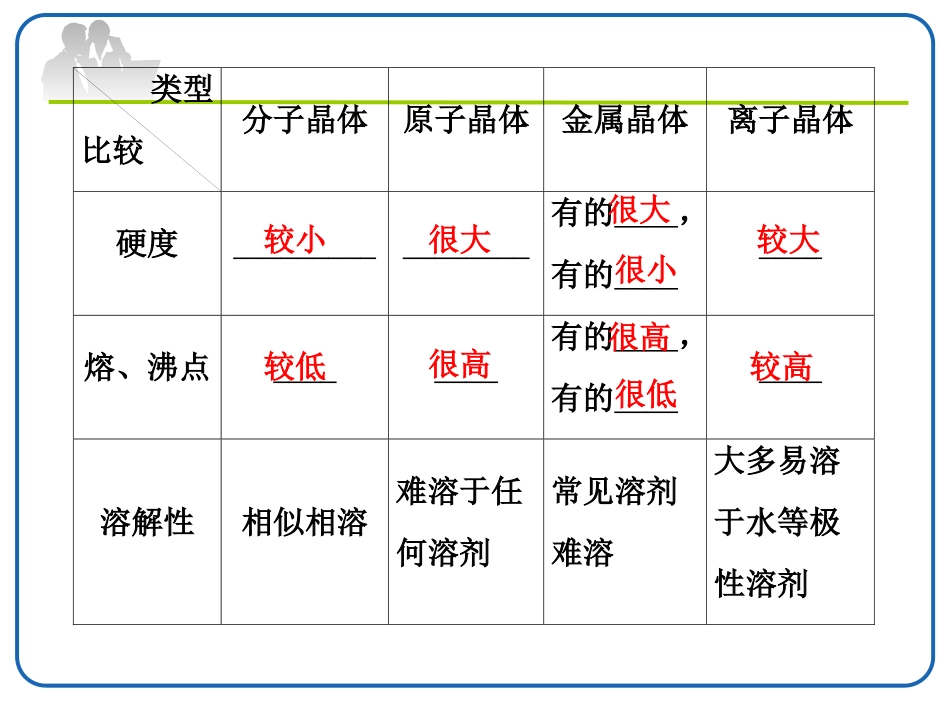
晶体的熔、沸点比较独立自学四种晶体类型的比较类型比较分子晶体原子晶体金属晶体离子晶体构成粒子_____________金属阳离子、自由电子_________粒子间的相互作用力_________(某些含氢键)__________________________分子原子阴、阳离子范德华力共价键金属键离子键类型比较分子晶体原子晶体金属晶体离子晶体硬度_________________有的____,有的________熔、沸点________有的____,有的________溶解性相似相溶难溶于任何溶剂常见溶剂难溶大多易溶于水等极性溶剂较小很大很大很小较大较低很高很高很低较高类型比较分子晶体原子晶体金属晶体离子晶体导电、传热性一般不导电,溶于水后有的导电一般不具有导电性,个别为半导体电和热的良导体晶体不导电,水溶液或熔融态导电物质类别及举例大多数非金属单质、气态氢化物、酸、非金属氧化物(SiO2除外)、绝大多数有机物(有机盐除外)部分非金属单质(如金刚石、硅、晶体硼),部分非金属化合物(如SiC、SiO2)金属单质与合金(如Na、Al、Fe、青铜)金属氧化物(如K2O、Na2O)、强碱(如KOH、NaOH)、绝大部分盐(如NaCl)判断晶体类型的五个依据1.构成晶体的微粒和微粒间的作用力;2.物质的类别;3.晶体的熔点;4.物质的导电性;5.硬度和机械性能
引导探究1、不同状态物质晶体熔、沸点的比较在相同条件下,不同状态物质的熔、沸点高低是不同的,一般有固体>液体>气体晶体熔沸点的比较例如:KBr(固体)>Br2(液体)>HBr(气体)引导探究2、不同类型晶体熔、沸点的比较(1)不同类型晶体的熔、沸点高低的一般规律:__________>____________>__________
(2)金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低