1 计算题:1) 写对化学反应方程式
2) 固体中常会有杂质,要分清参与分应是哪部分
3) 溶液参与反应时,只是溶质反应,水不参与,要搞清质量问题
4) 求反应后溶质质量分数时,除计入反应生成物后,还要注意反应物是否有其它可溶性杂质
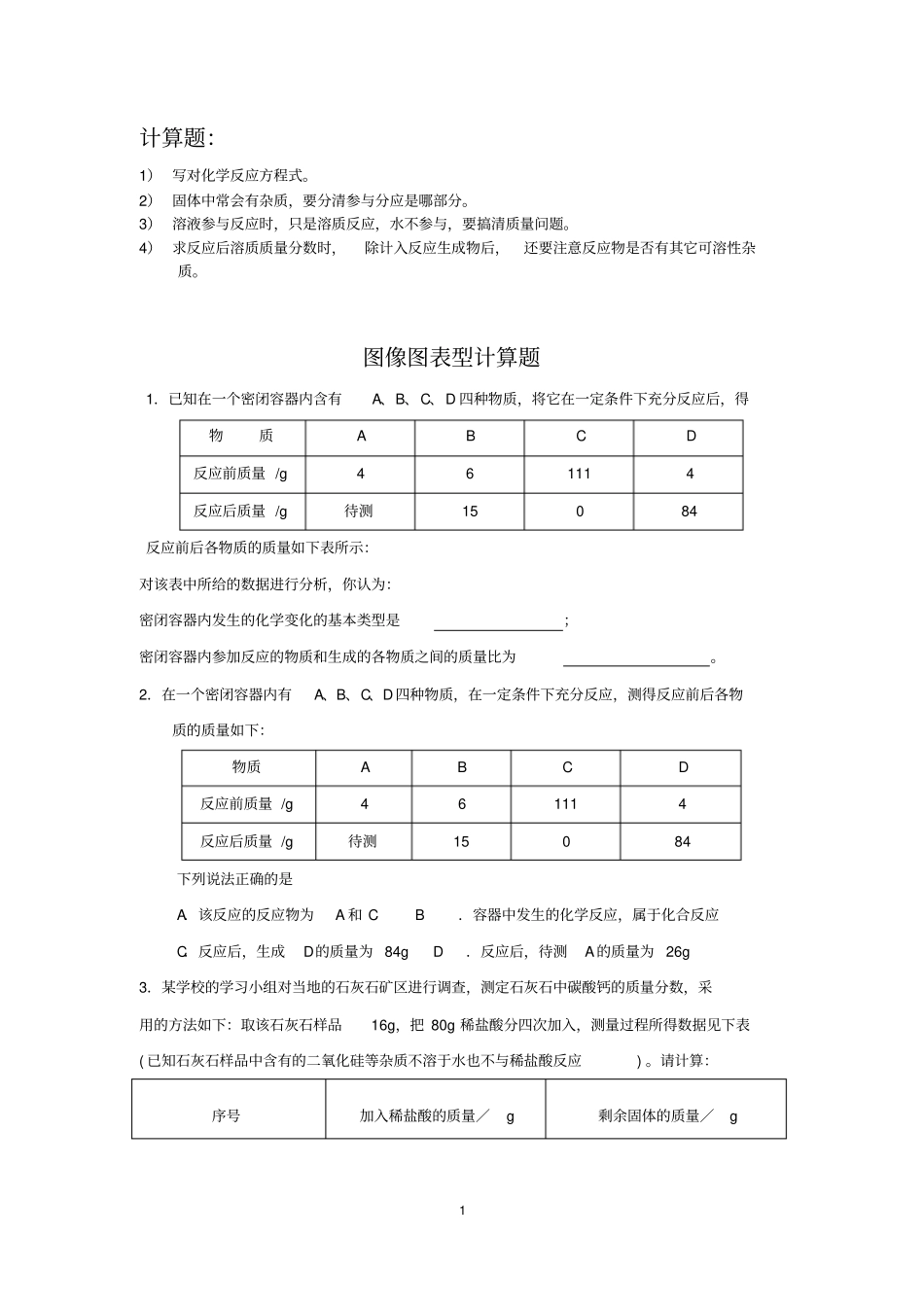
图像图表型计算题1.已知在一个密闭容器内含有A、B、C、D 四种物质,将它在一定条件下充分反应后,得反应前后各物质的质量如下表所示:对该表中所给的数据进行分析,你认为:密闭容器内发生的化学变化的基本类型是;密闭容器内参加反应的物质和生成的各物质之间的质量比为
2.在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:物质A B C D 反应前质量 /g 4 6 111 4 反应后质量 /g 待测15 0 84 下列说法正确的是A.该反应的反应物为A 和 C B.容器中发生的化学反应,属于化合反应C.反应后,生成D的质量为 84g D.反应后,待测A的质量为 26g 3.某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把 80g 稀盐酸分四次加入,测量过程所得数据见下表( 已知石灰石样品中含有的二氧化硅等杂质不溶于水也不与稀盐酸反应)
请计算:序号加入稀盐酸的质量/g 剩余固体的质量/g 物质A B C D 反应前质量 /g 4 6 111 4 反应后质量 /g 待测15 0 84 2 第 1 次20 12 第 2 次20 8 第 3 次20 4
8 第 4 次20 n (1) 上表中 n 的数值为 ___________
(2)石灰石中碳酸钙的质量分数为
(3) 求盐酸中溶质的质量分数(写出计算过程)
4.为测定石灰石中碳酸钙的含量,某学校课外小组同学做了如下实验:首先称取50 g 该地区的石灰石样品,然后将150 mL 的稀盐酸分5 次