物化公式归纳第一章化学热力学基础公式总结1
体积功We = -Pe△V2.热力学第一定律的数学表达式△ U = Q + W3. n mol 理想气体的定温膨胀过程途径 1 : 向真空膨胀Pe = 0 ,W1=0 途径 2: 一次恒外压膨胀 Pe = P2 途径 3: 无限缓慢膨胀 Pe = P1 - dP=P
定温可逆时 :Wmax=-Wmin= 4
焓定义式 H = U + PV在封闭体系中, W′= 0 ,体系发生一定容过程Qv = △ U 在封闭体系中, W′= 0 ,体系发生一定压过程Qp = H2 – H1 = △H 5
摩尔热容 Cm ( J · K- 1· mol -1 ): 定容热容 CV (适用条件 : 封闭体系、无相变、无化学变化、 W′=0 定容过程适用对象 : 任意的气体、液体、固体物质)定压热容 Cp (适用条件 : 封闭体系、无相变、无化学变化、 W′=0 的定压过程适用对象 : 任意的气体、液体、固体物质)单原子理想气体: Cv,m = , Cp,m = 双原子理想气体: Cv,m = , Cp,m = 多原子理想气体: Cv,m = 3R , Cp,m = 4R1221lnlnPPnRTVVnRT)(1222VVPW12213lnlnPPnRTVVnRTWnCCm21,TTmV dTnCUCp,m = Cv,m + R 6
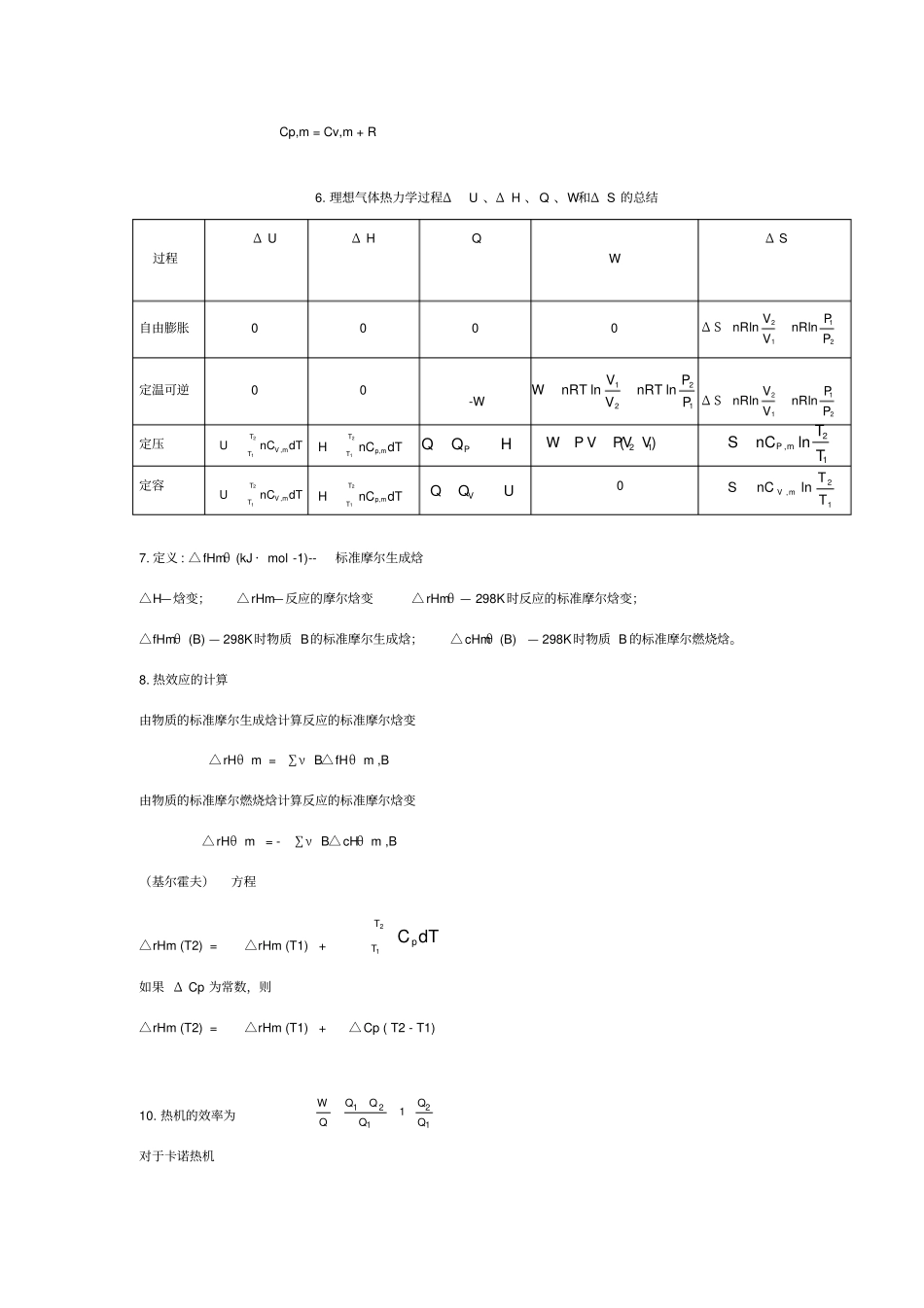
理想气体热力学过程ΔU 、Δ H 、 Q 、W和Δ S 的总结过程Δ UΔ HQWΔ S自由膨胀0000定温可逆00-W定压定容07
定义 : △ fHmθ (kJ · mol -1)-- 标准摩尔生成焓△H—焓变;△ rHm—反应的摩尔焓变△ rHmθ — 298K时反应的标准摩尔焓变;△fHmθ (B) — 298K时物质 B的标准摩尔生成焓;△ cHmθ (B) — 298K时物质 B 的标准摩尔燃烧焓