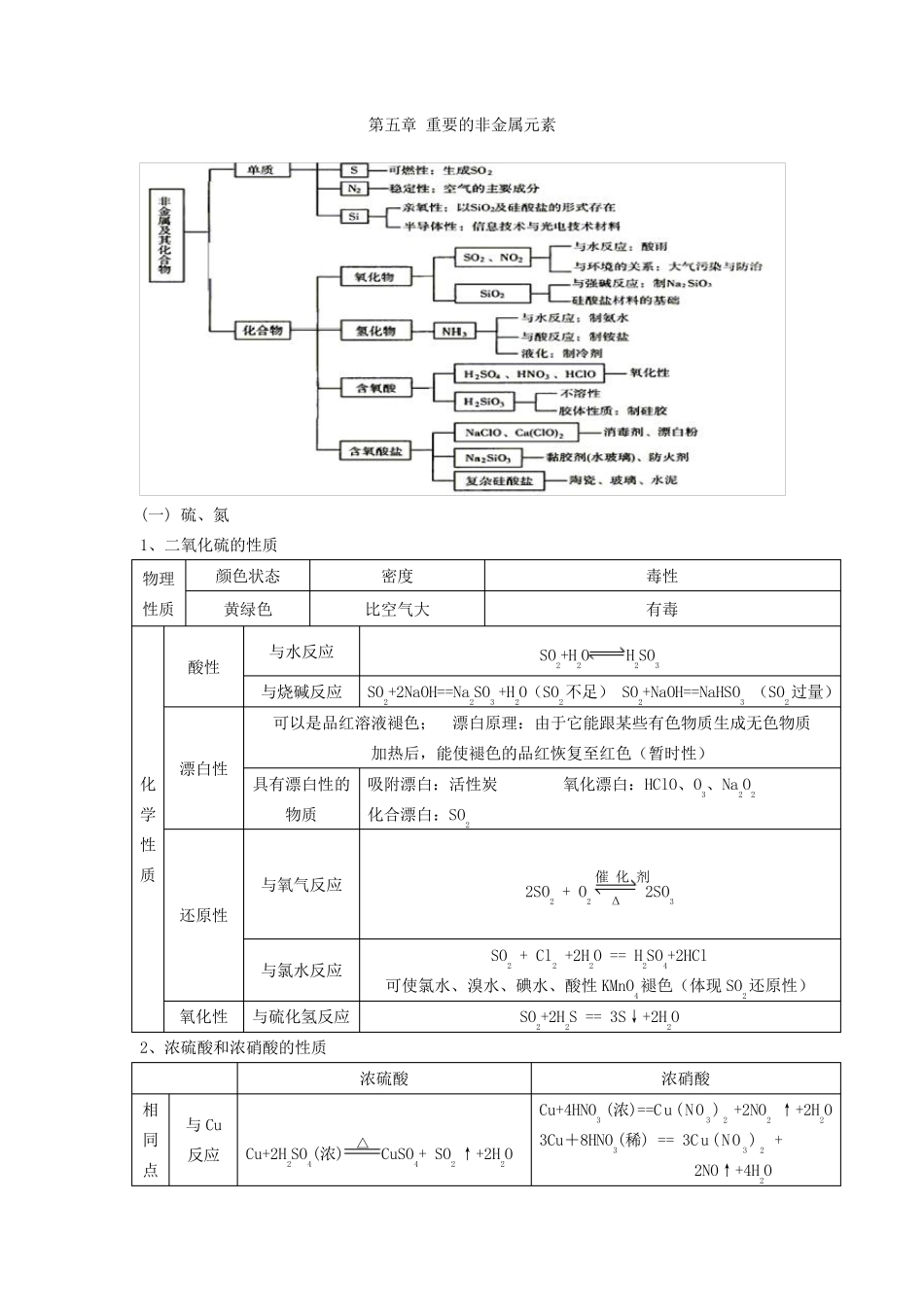
第五章 重要的非金属元素 (一) 硫、氮 1、二氧化硫的性质 物理性质 颜色状态 密度 毒性 黄绿色 比空气大 有毒 化学性质 酸性 与水反应 SO2+H2OH2SO3 与烧碱反应 SO2+2NaOH==Na2SO3 +H2O(SO2不足) SO2+NaOH==NaHSO3 (SO2过量) 漂白性 可以是品红溶液褪色; 漂白原理:由于它能跟某些有色物质生成无色物质 加热后,能使褪色的品红恢复至红色(暂时性) 具有漂白性的物质 吸附漂白:活性炭 氧化漂白:HClO、O3、Na2O2 化合漂白:SO2 还原性 与氧气反应 2SO2 + O2 2SO3 与氯水反应 SO2 + Cl2 +2H2O == H2SO4+2HCl 可使氯水、溴水、碘水、酸性KMnO4褪色(体现SO2还原性) 氧化性 与硫化氢反应 SO2+2H2S == 3S↓+2H2O 2、浓硫酸和浓硝酸的性质 浓硫酸 浓硝酸 相同点 与Cu反应 Cu+2H2SO4(浓)CuSO4+ SO2 ↑+2H2O Cu+4HNO3 (浓)==Cu(NO3)2 +2NO2 ↑+2H2O 3Cu+8HNO3(稀) == 3Cu(NO3)2 + 2NO↑+4H2O △ 催化剂 Δ 与木炭反应 C + 2H2SO4(浓) CO2↑+2SO2↑+2H2O C+4HNO3(浓)CO2↑+4NO2↑+2H2O 与铁铝反应 发生钝化现象,所以可以用铁制或铝制容器来存放冷的浓硫酸和浓硝酸 特性 ①吸水性 ②脱水性 ③强氧化性 ①强氧化性 ②漂白性 氮 1
氮— — 重要的非金属元素 (1)氮元素在自然界中的存在 ①游离态:主要以氮分子的形式存在于空气中
②化合态:部分存在于动植物体内的蛋白质中;部分存在于土壤、海洋里的硝酸盐和铵盐中
氮气 (1)氮分子内两个氮原子间以共价三键(N≡N)结合,断开该化学键需要较多的能量,所以氮气的化学性质