有机化合物中碳子的成键特点 教学目标:1、碳原子的成键特点 2、有机分子的空间构型和有机物中碳原子的成键特点的关系 3、有机化合物结构的表示方法:结构式、结构简式、键线式 知识分析 (一)有机物的特点: ①构成有机物质元素少(C、H、O、N、S、P),但有机物种类繁多,结构复杂
②大多数有机物难溶于水而易溶于汽油、酒精、苯等有机溶剂
③绝大多数有机物受热易分解,而且容易燃烧
④绝大多数有机物是非电解质,不易导电,熔点低
⑤有机物所起的化学反应比较复杂,一般比较慢,并且还常伴随有副反应发生
(二)有机物中碳原子的成键特点 碳原子位于周期表第Ⅳ主族第二周期,碳原子最外层有 4个电子,碳原子既不易失电子、也不易得电子
有机物种类繁多的原因,主要是由 C原子的结构决定的
其成键特点是: (1)在有机物中,碳原子有 4个价电子,碳呈四价,价键总数为4
(成键数目多) (2)碳原子既可与其它原子形成共价键,碳原子之间也可相互成键,既可以形成单键,也可以形成双键或三键
(成键方式多) ①碳原子间的成键方式:C—C、C=C、C≡C ②有机物中常见的共价键:C—C、C=C、C≡C、C—H、C—O、C—X、C=O、C≡N、C—N、苯环
③在有机物分子中,仅以单键方式成键的碳原子称为饱和碳原子;连接在双键、叁键或在苯环上的碳原子(所连原子的数目少于 4)称为不饱和碳原子
④C—C单键可以旋转而 C=C不能旋转(或三键)
(3)多个碳原子可以相互结合成长短不一的碳链和碳环,碳链和碳环还可以相互结合
{知识回顾} 1、共价键的定义:原子间通过共用电子对所形成的相互作用
2、共价键的类型: ①非极性键:由同种非金属原子组成,共用电子对处在成键原子中间
如: ②极性键:由不同种非金属原子组成,电子对偏向于成键原子非金属性强的一方
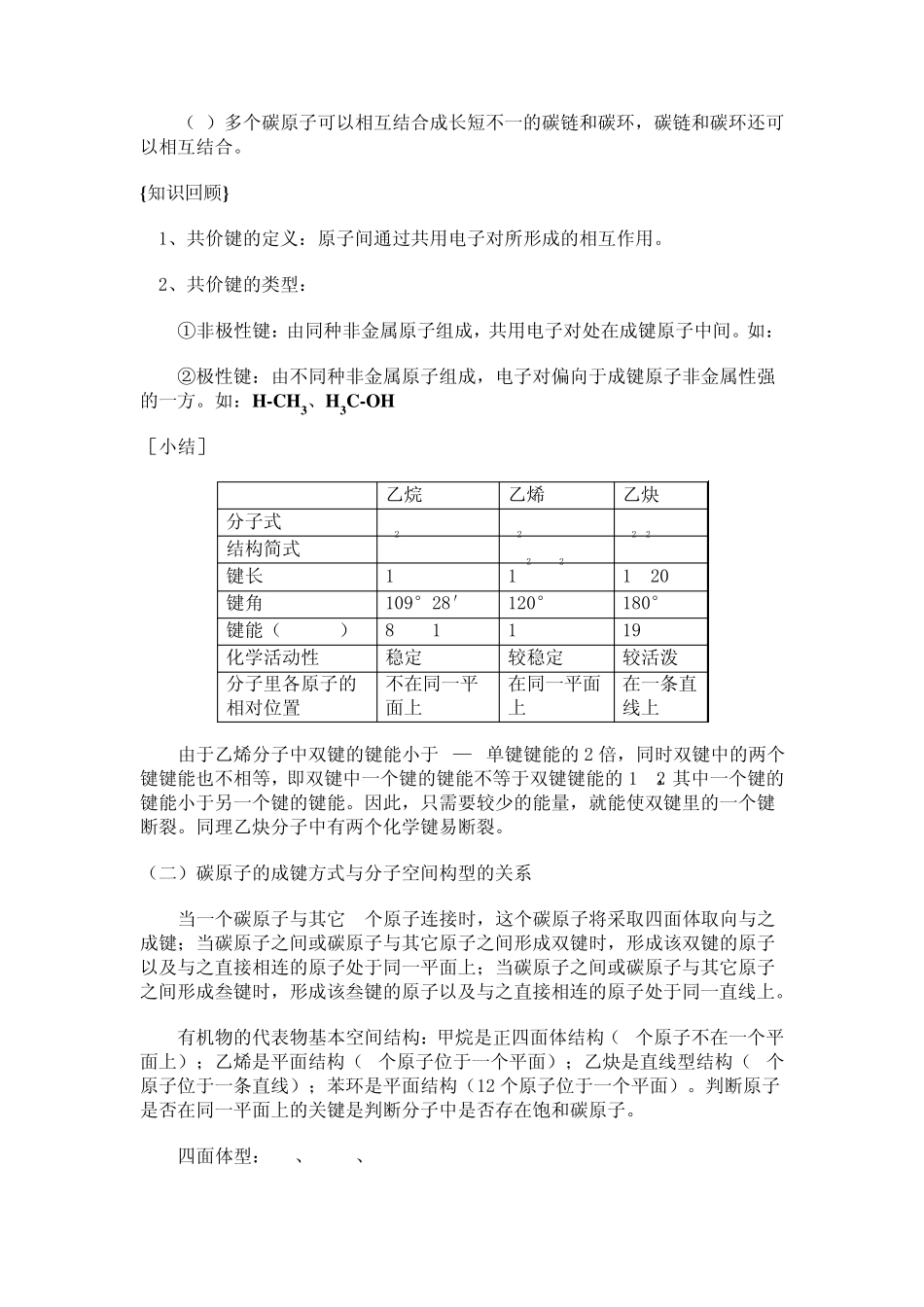
如:H-CH3、H3C-OH [小结] 乙烷 乙烯 乙