1 第二章配合物的结构及异构现象第一节配位数与配位多面体配位多面体: 把围绕中心原子的配位原子看作点,以线按一定的方式连接各点就得到配位多面体
用来描述中心离子的配位环境
1、配位数为 2 一般为直线型结构,如: H3N— Ag— NH 3大多限于 Cu(I)、Ag(I) 、Au(I) 和 Hg(II) 的配合物
如: [CuCl 2]-,[Au(CN) 2]-2、配位数为 3 一般为等边三角形结构
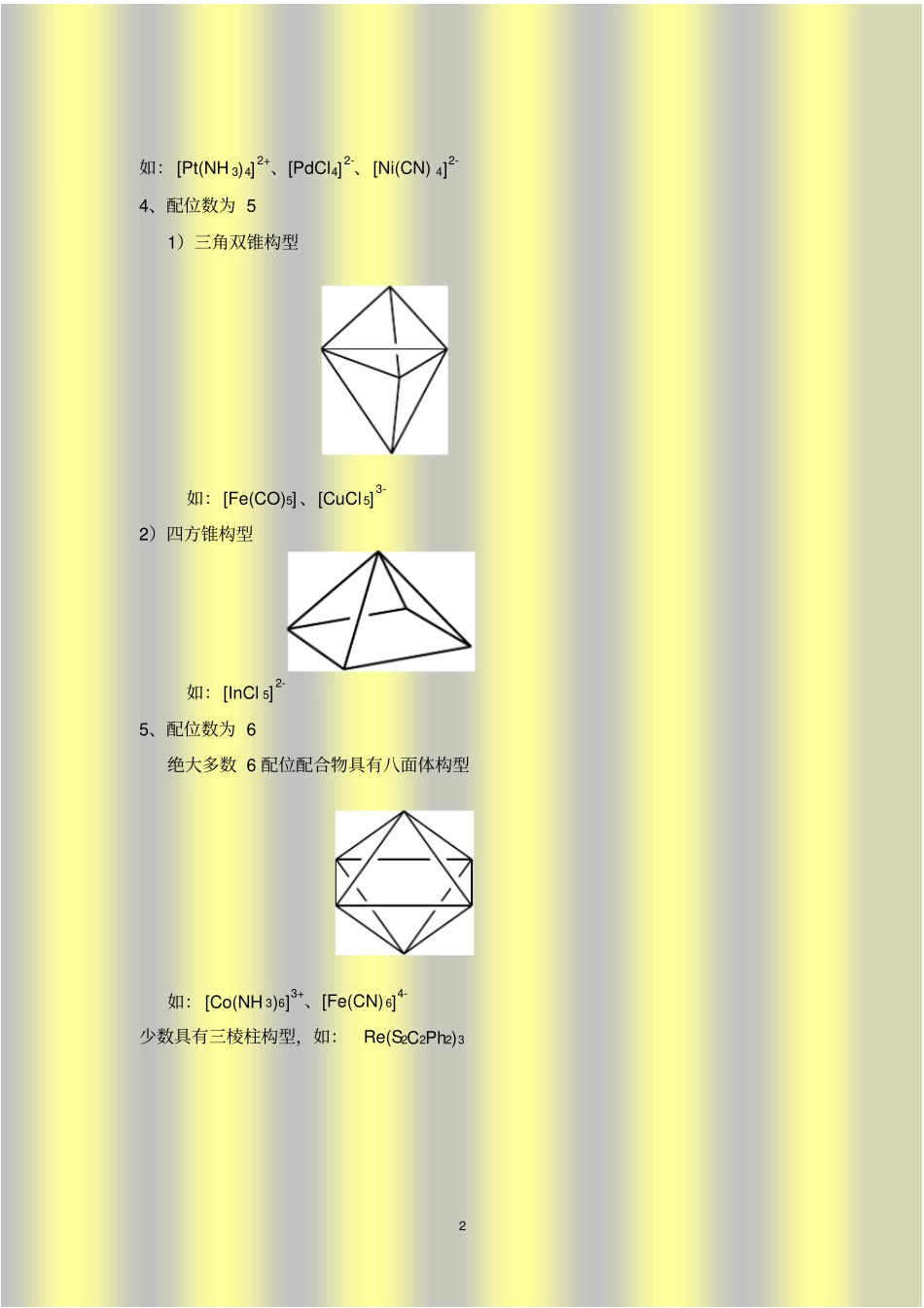
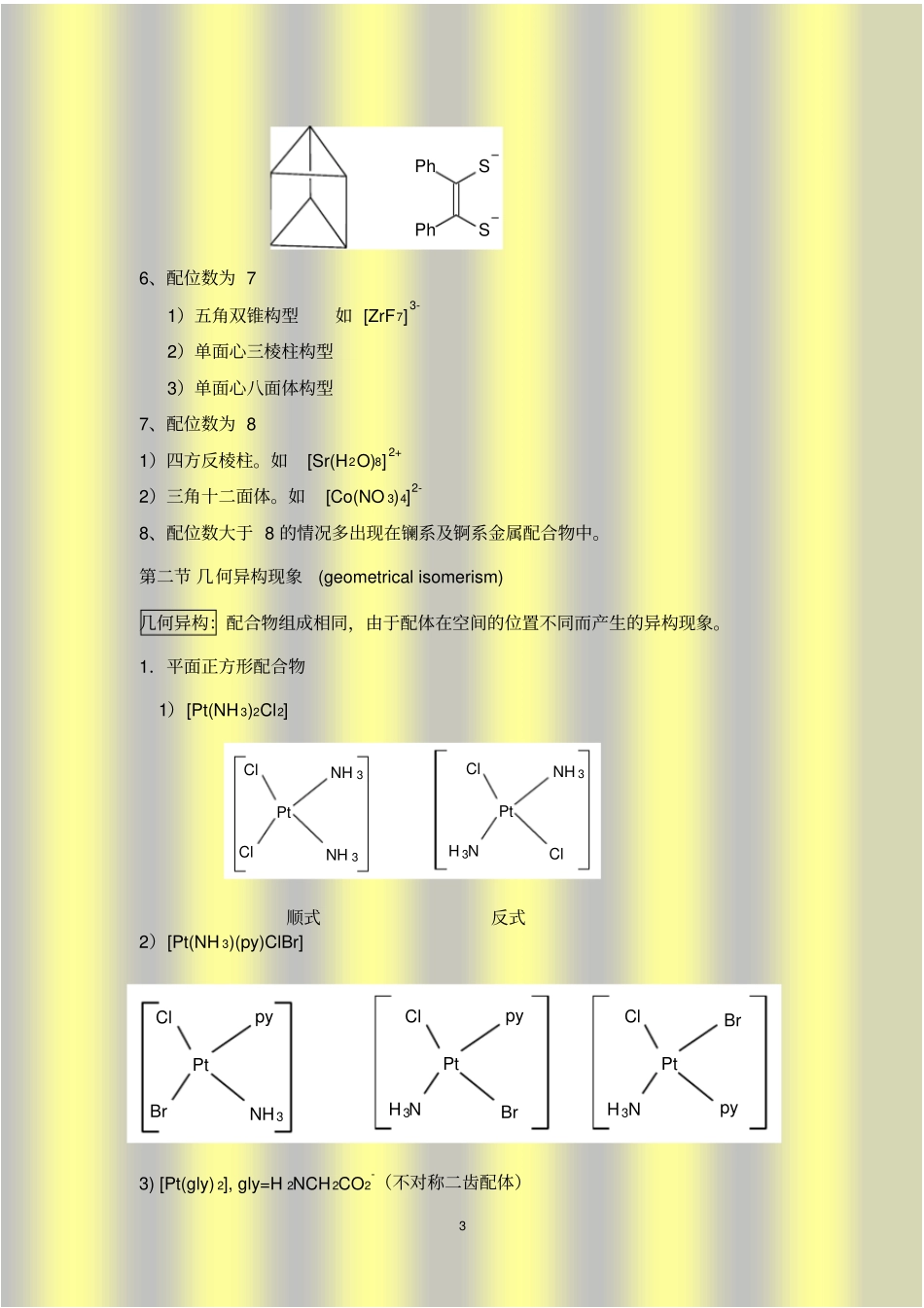
如: [HgI 3]-、[Pt(PPh3)3]3、配位数为 4 1)四面体构型如: [Zn(NH 3)4]2+、[CoCl 4]2-、[NiCl 4]2-2) 平面正方形构型2 如: [Pt(NH 3)4]2+、[PdCl4]2-、[Ni(CN) 4]2-4、配位数为 5 1)三角双锥构型如:[Fe(CO)5] 、[CuCl 5]3-2)四方锥构型如:[InCl 5]2-5、配位数为 6 绝大多数 6 配位配合物具有八面体构型如: [Co(NH 3)6]3+、[Fe(CN) 6]4-少数具有三棱柱构型,如:Re(S2C2Ph2)3 3 PhSSPh6、配位数为 7 1)五角双锥构型如 [ZrF7]3-2)单面心三棱柱构型3)单面心八面体构型7、配位数为 8 1)四方反棱柱
如[Sr(H2O)8]2+2)三角十二面体
如[Co(NO 3)4]2-8、配位数大于 8 的情况多出现在镧系及锕系金属配合物中
第二节 几何异构现象(geometrical isomerism) 几何异构:配合物组成相同,由于配体在空间的位置不同而产生的异构现象
1.平面正方形配合物1)[Pt(NH 3)2Cl2] 顺式反式2)[Pt(NH 3)(py)ClBr] 3) [Pt(gly) 2], gly=H 2NCH 2CO2-(不对称二齿配体)NH 3ClPtNH 3ClNH 3ClPtClH 3NpyC