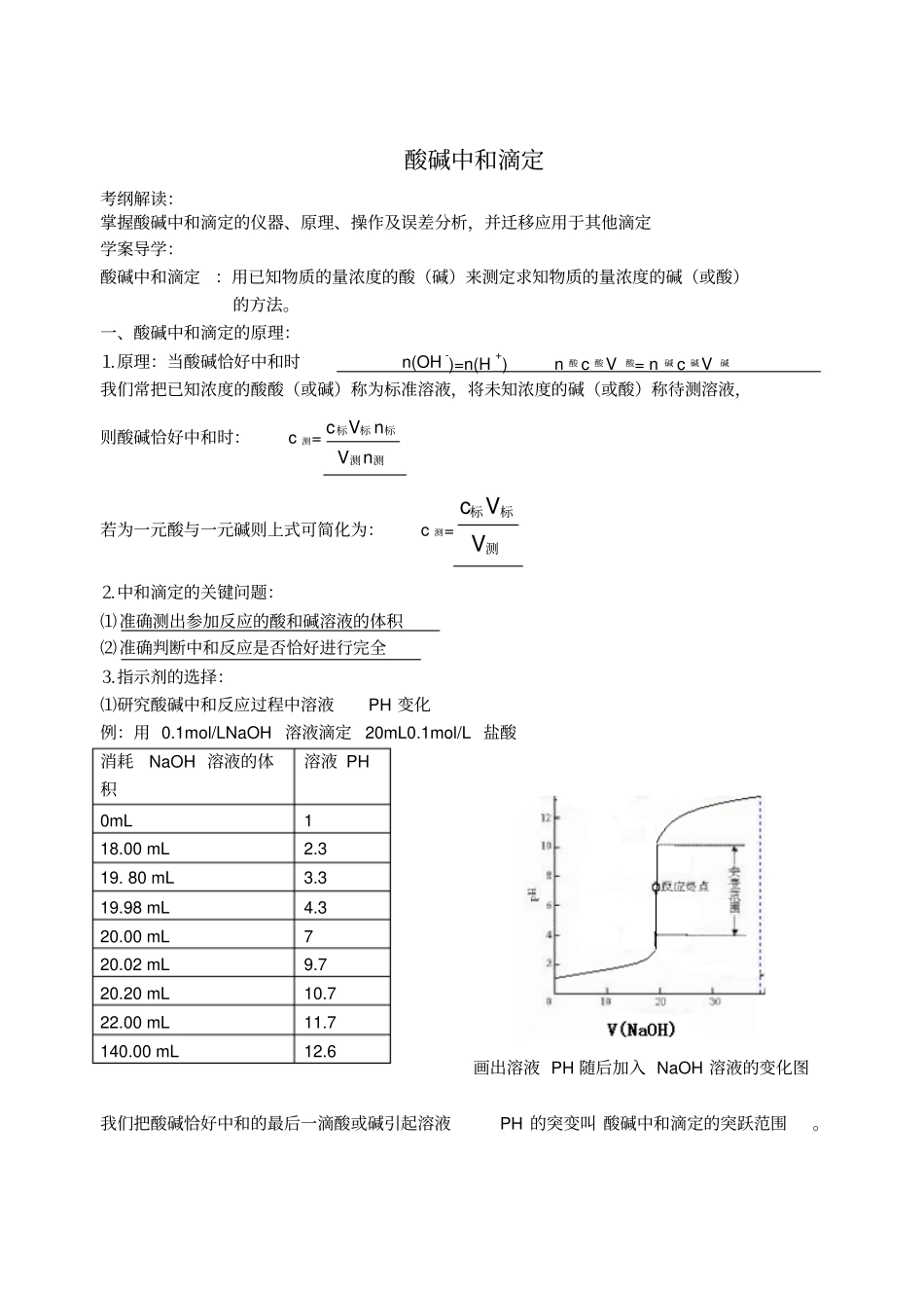
酸碱中和滴定考纲解读:掌握酸碱中和滴定的仪器、原理、操作及误差分析,并迁移应用于其他滴定学案导学:酸碱中和滴定:用已知物质的量浓度的酸(碱)来测定求知物质的量浓度的碱(或酸)的方法
一、酸碱中和滴定的原理:⒈原理:当酸碱恰好中和时n(OH-)=n(H+) n 酸 c 酸V酸= n 碱 c 碱V碱我们常把已知浓度的酸酸(或碱)称为标准溶液,将未知浓度的碱(或酸)称待测溶液,则酸碱恰好中和时:c 测=测测标标标nVnVc若为一元酸与一元碱则上式可简化为:c 测=测标标VVc⒉中和滴定的关键问题:⑴准确测出参加反应的酸和碱溶液的体积⑵准确判断中和反应是否恰好进行完全⒊指示剂的选择:⑴研究酸碱中和反应过程中溶液PH 变化例:用 0
1mol/LNaOH 溶液滴定 20mL0
1mol/L 盐酸画出溶液 PH 随后加入 NaOH 溶液的变化图我们把酸碱恰好中和的最后一滴酸或碱引起溶液PH 的突变叫 酸碱中和滴定的突跃范围
消耗NaOH 溶液的体积溶液 PH 0mL 1 18
00 mL 2
80 mL 3
98 mL 4
00 mL 7 20
02 mL 9
20 mL 10
00 mL 11
00 mL 12
6 ⑵指示剂的选择是根据突跃范围①若用强碱滴定强酸突跃范围: 4
7 甲基橙( 3
4)从色变为色时说明达到了滴定终点酚酞( 8
2—— 10
)从色变为色时说明达到了滴定终点注意: 酸碱中和滴定不选石蕊作指示滴定终点,因其PH 变色范围宽, 颜色不易觉察,误差超过了酸碱中和滴定允许的误差
②若用强酸滴定强碱突跃范围: 9
3 甲基橙( 3
4)从色变为色时说明达到了滴定终点酚酞( 8
2—— 10
)从色变为色时说明达到了滴定终点③若用强酸滴定弱碱:如用盐酸滴定氨