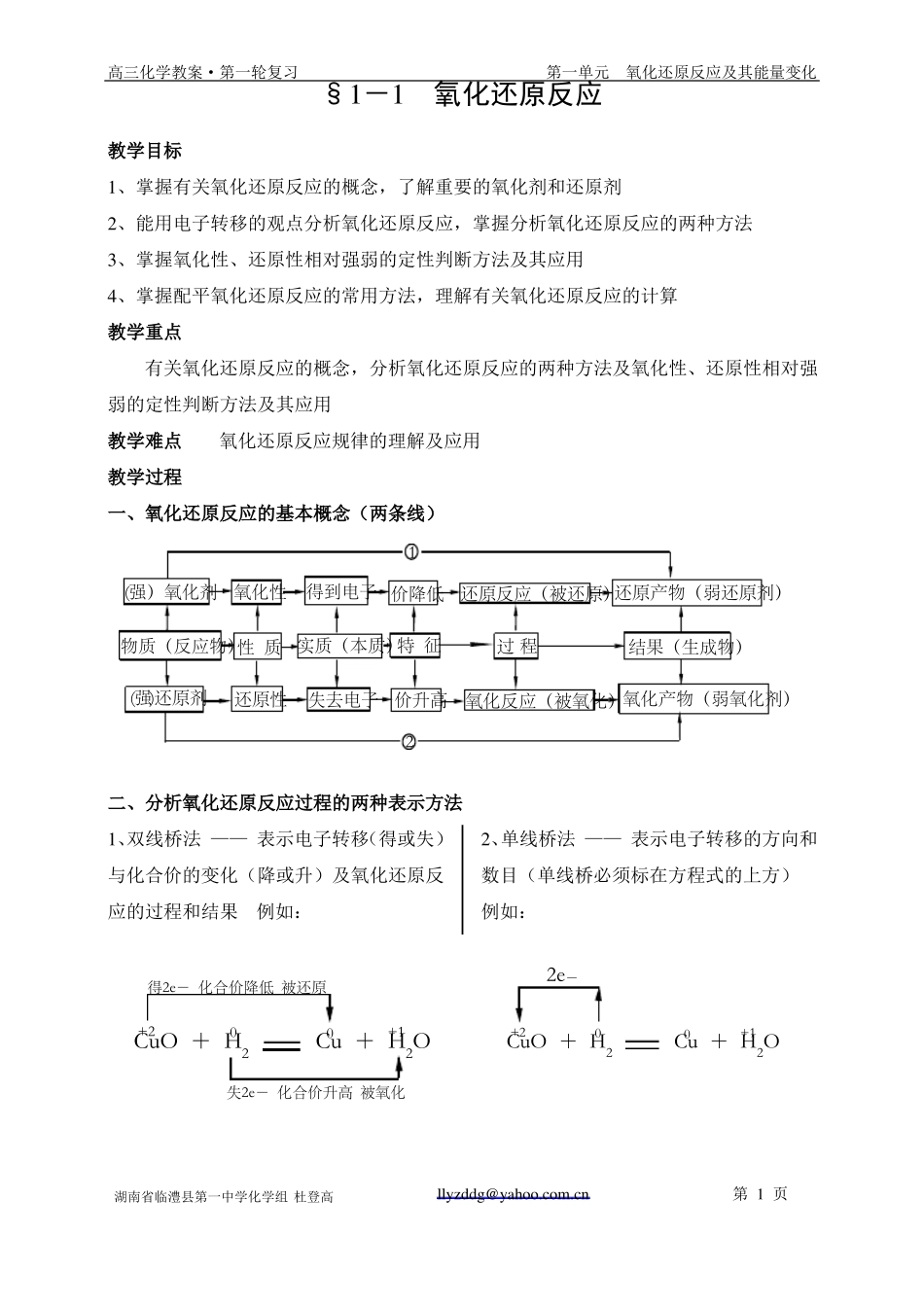
高三化学教案·第一轮复习第一单元氧化还原反应及其能量变化§1-1氧化还原反应教学目标1、掌握有关氧化还原反应的概念,了解重要的氧化剂和还原剂2、能用电子转移的观点分析氧化还原反应,掌握分析氧化还原反应的两种方法3、掌握氧化性、还原性相对强弱的定性判断方法及其应用4、掌握配平氧化还原反应的常用方法,理解有关氧化还原反应的计算教学重点有关氧化还原反应的概念,分析氧化还原反应的两种方法及氧化性、还原性相对强弱的定性判断方法及其应用教学难点氧化还原反应规律的理解及应用教学过程一、氧化还原反应的基本概念(两条线)1(强)氧化剂氧化性得到电子 价降低还原反应(被还原)还原产物(弱还原剂)过 程结果(生成物)氧化产物(弱氧化剂)物质(反应物)性 质实质(本质)特 征(强)还原剂还原性失去电子价升高氧化反应(被氧化)2二、分析氧化还原反应过程的两种表示方法1、双线桥法 —— 表示电子转移(得或失)与化合价的变化(降或升)及氧化还原反应的过程和结果例如:2、单线桥法 —— 表示电子转移的方向和数目(单线桥必须标在方程式的上方)例如:得2e- 化合价降低 被还原+200+1+22e-CuO + H20CuO + H2Cu + H2OCu + H2O0+1失2e- 化合价升高 被氧化湖南省临澧县第一中学化学组 杜登高llyzddg@yahoo
cn第 1 页高三化学教案·第一轮复习第一单元氧化还原反应及其能量变化分析物质:CuO 是氧化剂,具有氧化性,被还原为 Cu (还原产物是 Cu )H2是还原剂,具有还原性,被氧化为 H2O(氧化产物是 H2O)分析元素:(必须指明元素所在的物质及该元素的存在价态)CuO 中Cu 是氧化剂,具有氧化性,被还原为 Cu 中CuH2 中 H 是还原剂,具有还原性,被氧化为 H2O 中 H归纳小结:氧化还原不可分,电子转移是根本,判断查看化合价,价降价升