第 1 页共 9 页(g)AH]=100
3kJ・molt①AH2=-11
0kJ・molt②AH3=kJ・molT
(2)某温度下,等物质的量的碘和环戊烯()在刚性容器内发生反应③,起始总压为F 图为刚性容器中,进料浓度2021 年高考化学总复习:化学平衡常数计算一
(2019 全国 II 卷)环戊二烯&
■'/)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产
回答下列问题:平衡时总压增加了 20%,环戊烯的转化率为,该反应的平衡常数 Kp=Pa
达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有(填标号)
通入惰性气体 B
增加环戊烯浓度 D
增加碘浓度2
(2019 全国 III 卷)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长
因此,将氯化氢转化为氯气的技术成为科学研究的热点
回答下列问题:(1)Deacon 发明的直接氧化法为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)
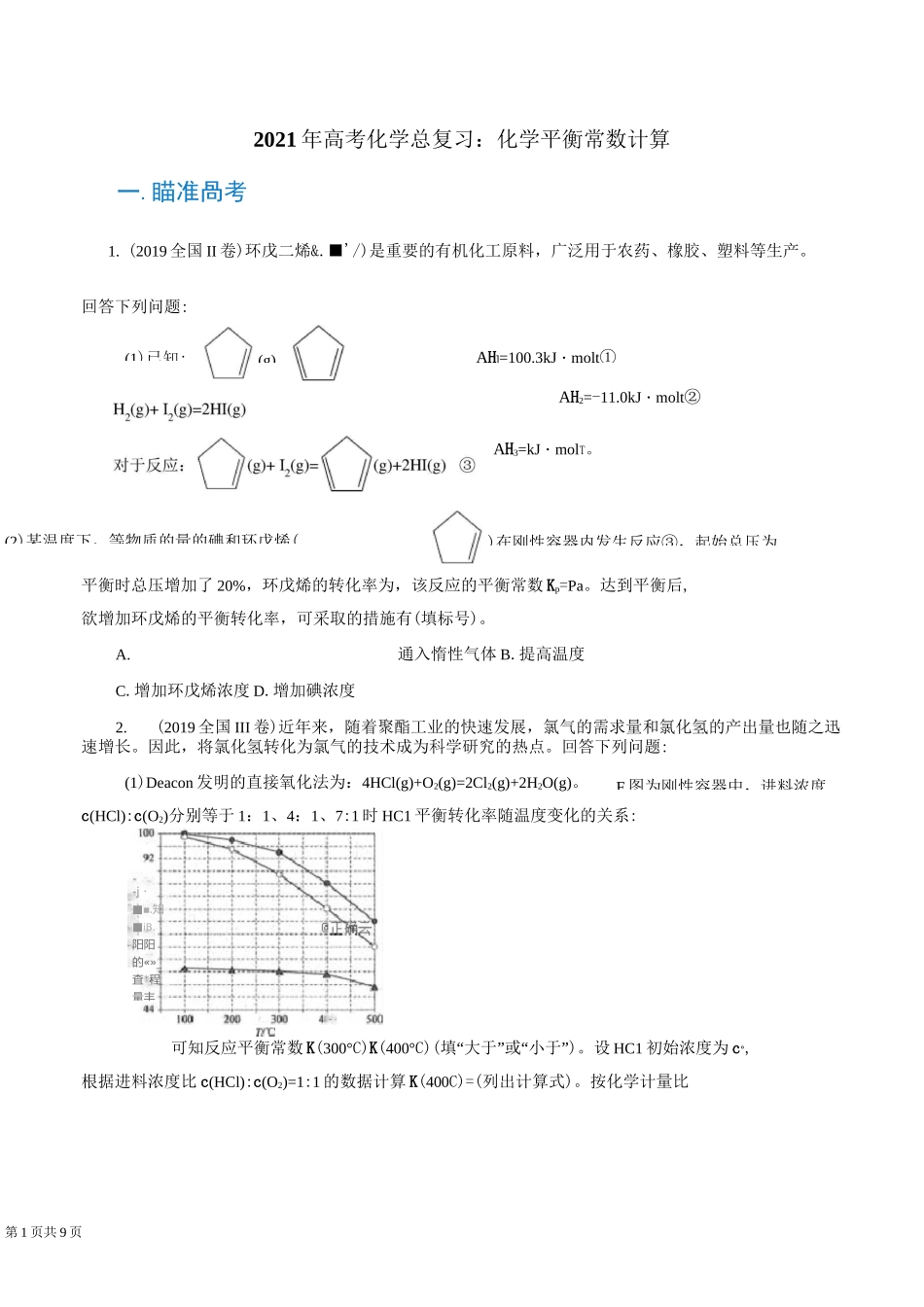
c(HCl):c(O2)分别等于 1:1、4:1、7:1 时 HC1 平衡转化率随温度变化的关系:可知反应平衡常数 K(300°C)K(400°C)(填“大于”或“小于”)
设 HC1 初始浓度为 c°,根据进料浓度比 c(HCl):c(O2)=1:1 的数据计算 K(400C)=(列出计算式)
按化学计量比(1)已知:C-j・■■
阳阳的«»_査*程量丰第 2 页共 9 页光LZ /\/V进料可以保持反应物高转化率,同时降低产物分离的能耗
进料浓度比 c(HCl):c(02)过低、过高的不利影响分别是
(2018 课标 II)CH4-CO2催化重整不仅可以得到合成气(CO 和 H2),还对温室气体的减排具有重要意义
回答下列问题:(1)CH4-CO2催化重整反应为:CH4(g)+CO2(