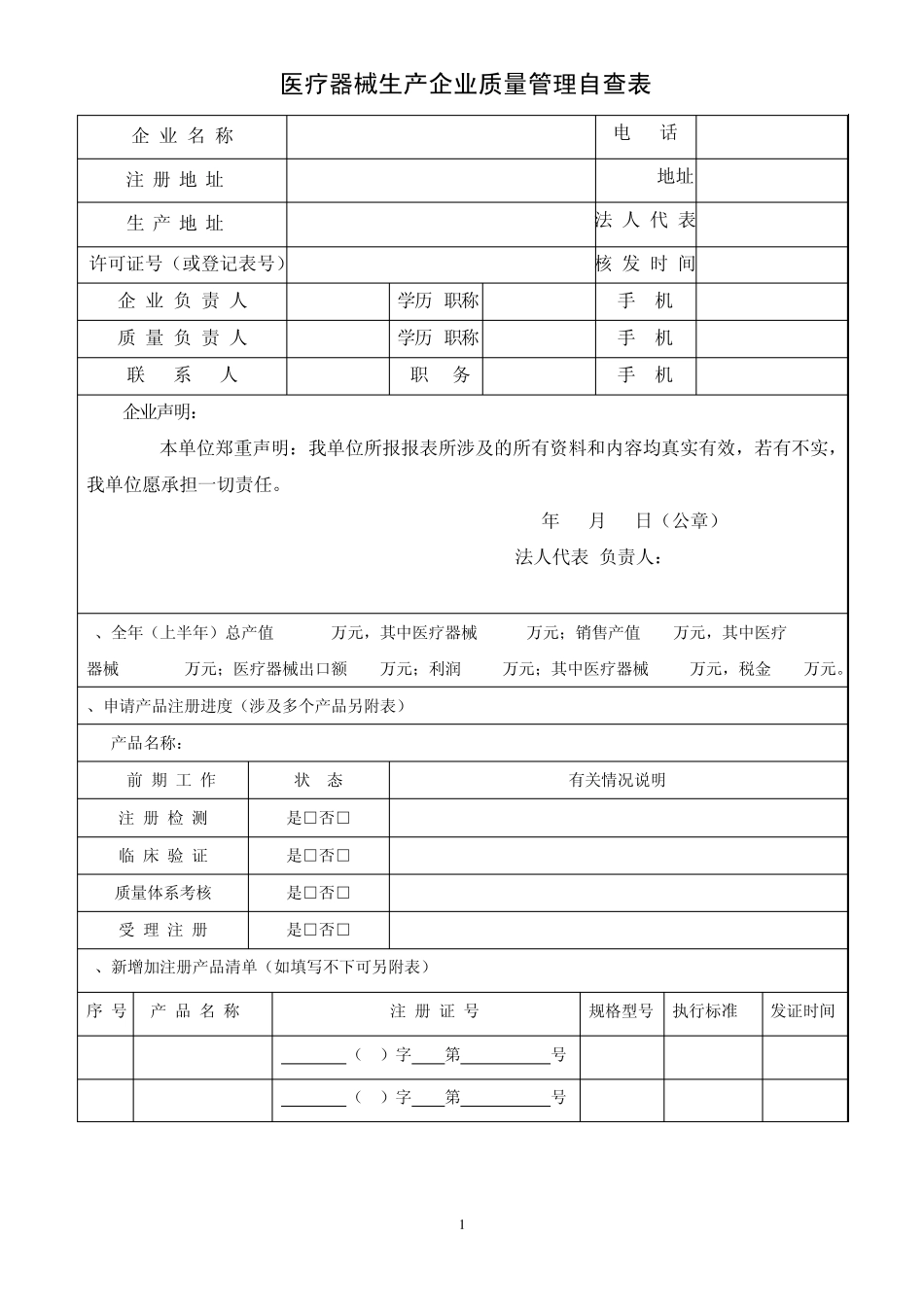
1 医疗器械生产企业质量管理自查表 企 业 名 称 电 话 注册地址 E-mail地址 生产地址 法 人 代 表 许可证号(或登记表号) 核 发 时 间 企 业 负 责 人 学历/职称 手 机 质 量 负 责 人 学历/职称 手 机 联 系 人 职 务 手 机 企业声明: 本单位郑重声明:我单位所报报表所涉及的所有资料和内容均真实有效,若有不实,我单位愿承担一切责任。 年 月 日(公章) 法人代表/负责人: 1、全年(上半年)总产值 万元,其中医疗器械 万元;销售产值 万元,其中医疗 器械 万元;医疗器械出口额 万元;利润 万元;其中医疗器械 万元,税金 万元。 22、申请产品注册进度(涉及多个产品另附表) 产品名称: 前 期 工 作 状 态 有关情况说明 注 册 检 测 是□否□ 临 床 验 证 是□否□ 质量体系考核 是□否□ 受 理 注 册 是□否□ 3、新增加注册产品清单(如填写不下可另附表) 序 号 产 品 名 称 注 册 证 号 规格型号 执行标准 发证时间 ( )字 第 号 ( )字 第 号 2 4、许可证与注册注册证情况说明: (1)生产许可证到期时限:□5年 □4年 □3年 □2年 □1年 □半年内(重新换证□是 □否) (2)有效注册产品 个, 其中:三类 个, 二类 个,一类 个。 (3)注册产品有效期限:四年 个,三年 个,二年 个,一年 个,半年内 个(重新注册□是 □否) 5、人员变动及企业生产条件(地址、场所、环境、检测)变化情况说明: 6、《医疗器械生产质量管理规范》(GMP)实施情况: (1)是否通过 GMP□是 □否(□无菌 □植入 □体外诊断试剂 □其它) (2)未实施 GMP的原因: 7、质量管理体系认证情况说明: (1)今年是否通过何种认证:□lSO13485 □CE □FDA □其它 □无 证书号: 通过时间: 年 月 日 覆盖范围和产品: (2)今年是否通过认证机构的监督审核:□是 □否,认证审核:□lSO13485 □CE □FDA □其它 审核时间: 年 月 日 审核机构: 8、产品上市质量跟踪情况(包括医疗器械不良事件监测): 9、产品监督抽查和行政处罚情况: 10、新产品开发情况: 11、意见和建议: 3 《医疗器械生产质量管理规范》 无菌医疗器械生产质量体系考核自查表 企业名称: 产品名称: 审查日期: 审查人员: 企业负责人: (签名) 4 一、评分标准 备注:1、 无菌医疗器械...