《医疗器械生产企业许可证》现场审查标准说明 一、一般要求 (一)根据《医疗器械监督管理条例》、《医疗器械生产监督管理办法》,结合现场审查的实际情况,特制定本标准
(二)本标准适用于对新开办企业申办《医疗器械生产企业许可证》、《医疗器械生产企业许可证》生产地址和生产范围变更以及《医疗器械生产企业许可证》换证的现场审查
医疗器械生产企业日常监督管理可参照执行本标准
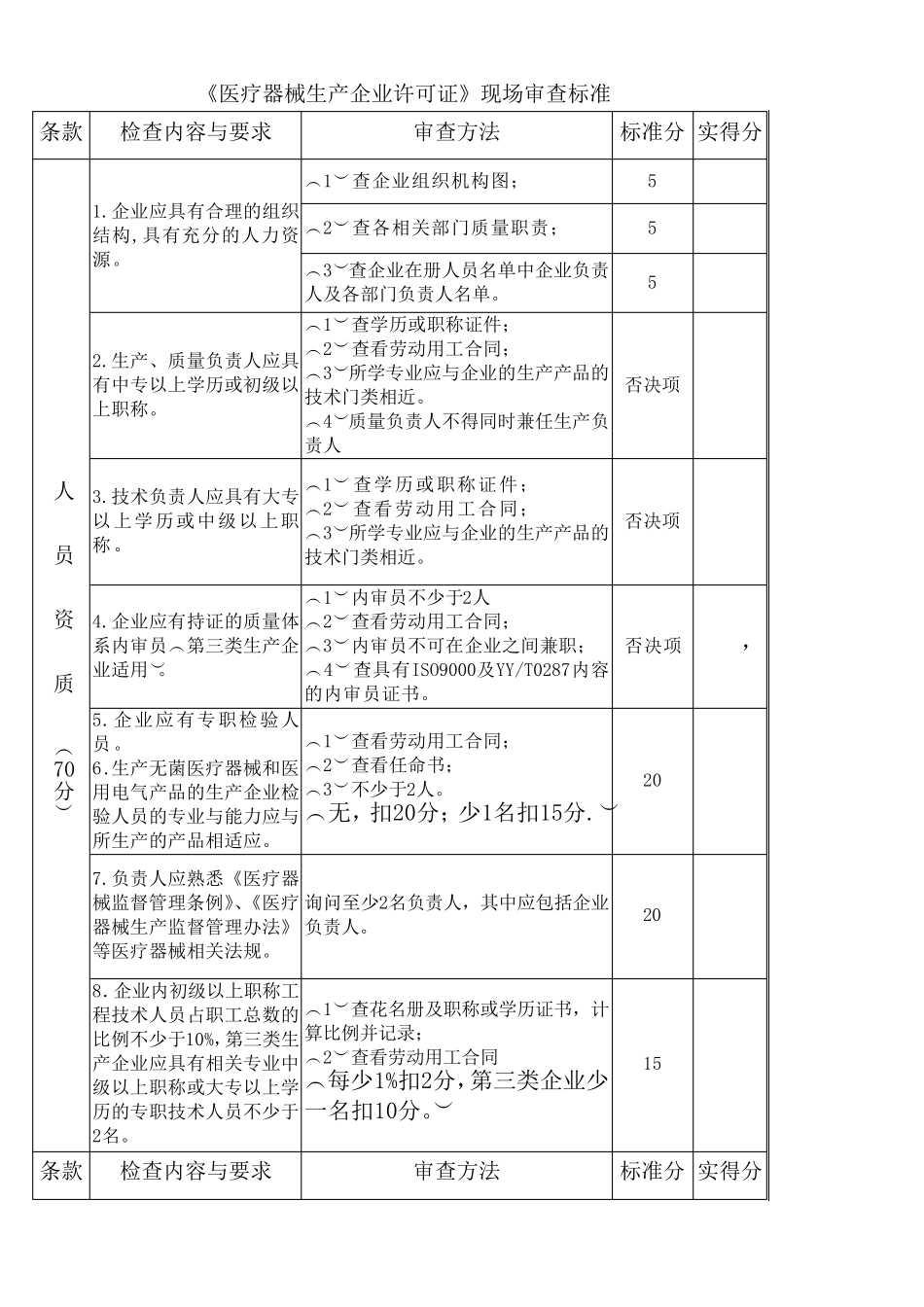
(三)生产企业现场审查按《〈医疗器械生产企业许可证〉现场审查评分表》进行,审查评分表分为 5个部分,其中否决条款 5项
评分条款总分为 300分,各部分内容和分值为: 1.人员资质 70分 2.场 地 80分 3.法规及质量管理文件 40分 4.生产能力 40分 5.检验能力 70分 (四)合格标准: “否决条款”一项不合格,即为本次审查不合格;“否决条款”全部合格且各部分的得分率均达到 80%以上为合格; “否决条款”全部合格且各部分的得分率均达到 60%以上,但其中一部分或几部分的得分率不足 80%的,要求企业整改并对整改情况进行复查,复查仍不合格的,即为本次审查不合格; “否决条款”全部合格但有一部分或几部分的得分率不足60%的,即为本次审查不合格
二、评分方法 (一)按审查评分表中审查方法评分
扣分时,最多至本项分数扣完为止
(二)按评分通则评分
评分不宜量化的条款, 按评分通则打分
实得分等于每项规定满分乘以得分系数
得分系数及含义: 1
0 全面达到规定要求; 0
8 执行较好,但仍需改进; 0
7 基本达到要求,部分执行较好; 0
6 基本达到要求; 0
5 已执行,但尚有一定差距; 0
0 未开展工作
(三)缺项(条)的处理:缺项(条)指由于产品管理类别而出现的合理缺项(条)
缺项(条)不记分,计算得分率时,从该项(条)标准总分中减去缺项(条)应得分
计算公式为: 得分率= 实得分/(该部