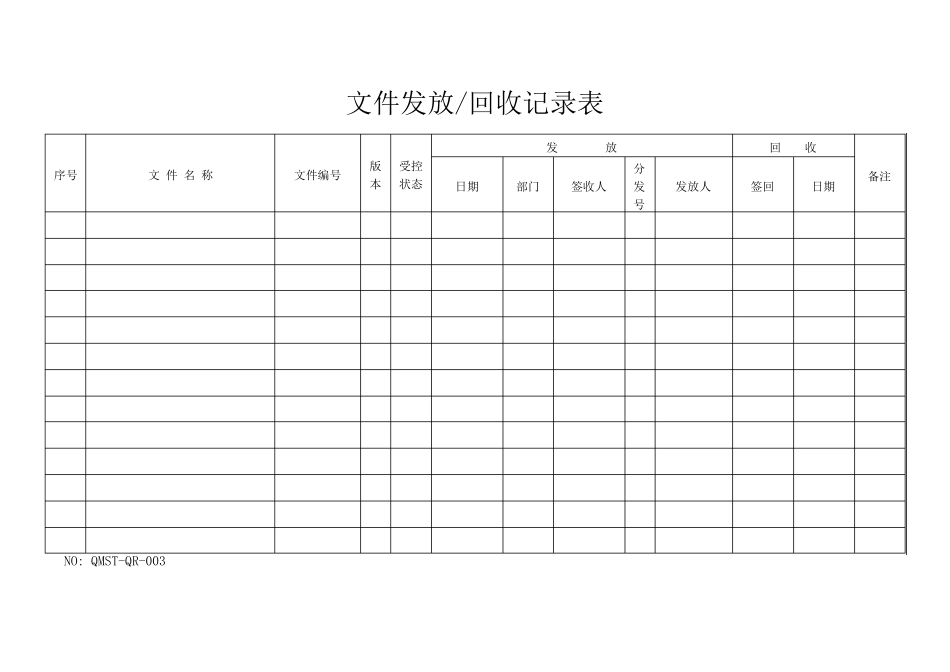
2018 年度内部审核与管理制度实施考核检查记录 被考核(审核)部门 考核(审核)时间 年 月 日 考核(审核)人 审核(考核)文件名称 考核(审核)内容及标准: 存在问题: 考核人签字: 年 月 日 整改措施: 被考核人签字: 年 月 日 备注 此表单适用于:质量管理体系文件审核、质量管理制度执行情况考核; 被考核部门负责人(签字) 使用部门: NO: QMST-QR-001 召回计划实施情况报告 产品名称 注册证号码 生产企业 中国境内负责单位、负责人及联系方式 召回工作联系人和 联系方式 通 知 情 况 承担召回联系 责任的收货人 应当通知人数 已通知人数 通知时间 通知方式 其他收货人 应当通知人数 已通知人数 通知时间 通知方式 完 成 情 况 应当召回数量 已完成数量 有效性检查情况 召回产品的处理措施 完成召回需要时间估计 NO: QMST-QR-002 文件发放/回收记录表 NO: QMST-QR-003 序号 文 件 名 称 文件编号 版本 受控状态 发 放 回 收 备注 日期 部门 签收人 分发号 发放人 签回 日期 文件更改申请审批记录表 部门 申请人及职务 文件名称: 文件编码 增订(修订)内容及理由: 修订前内容 修订后内容 部门意见: 签名: 日期: 年 月 日 质量管理部意见: 签名: 日期: 年 月 日 批准人意见: 签名: 日期: 年 月 日 备注:如增订内容较多可在附页上增加内容,并在修订内容后注明“见附页”
NO: QMST-QR-004 购进(采购)记录 序号 购货日期 商品名称 规格(剂型) 生产厂商 供货单位 数量 注册证号 (备案凭证编号) 单价 金额 采购员 备注 NO: QMST-QR-005 文件作废/保留/销毁单 NO: QMST-QR-006 序号 文 件 名 称 文件编号 分发号 受控状态 作废/保留/销毁 申请人