中考化学化学溶解度综合题及答案一、初中化学溶解度1
三种不含结晶水的固体物质甲、乙、丙的溶解度曲线如下图,卞列说法正确的是A
将"°C 时的三种物质的饱和溶液升温至 t2°C 时,所得溶液的的溶质质量分数大小顺序是乙>甲>丙B
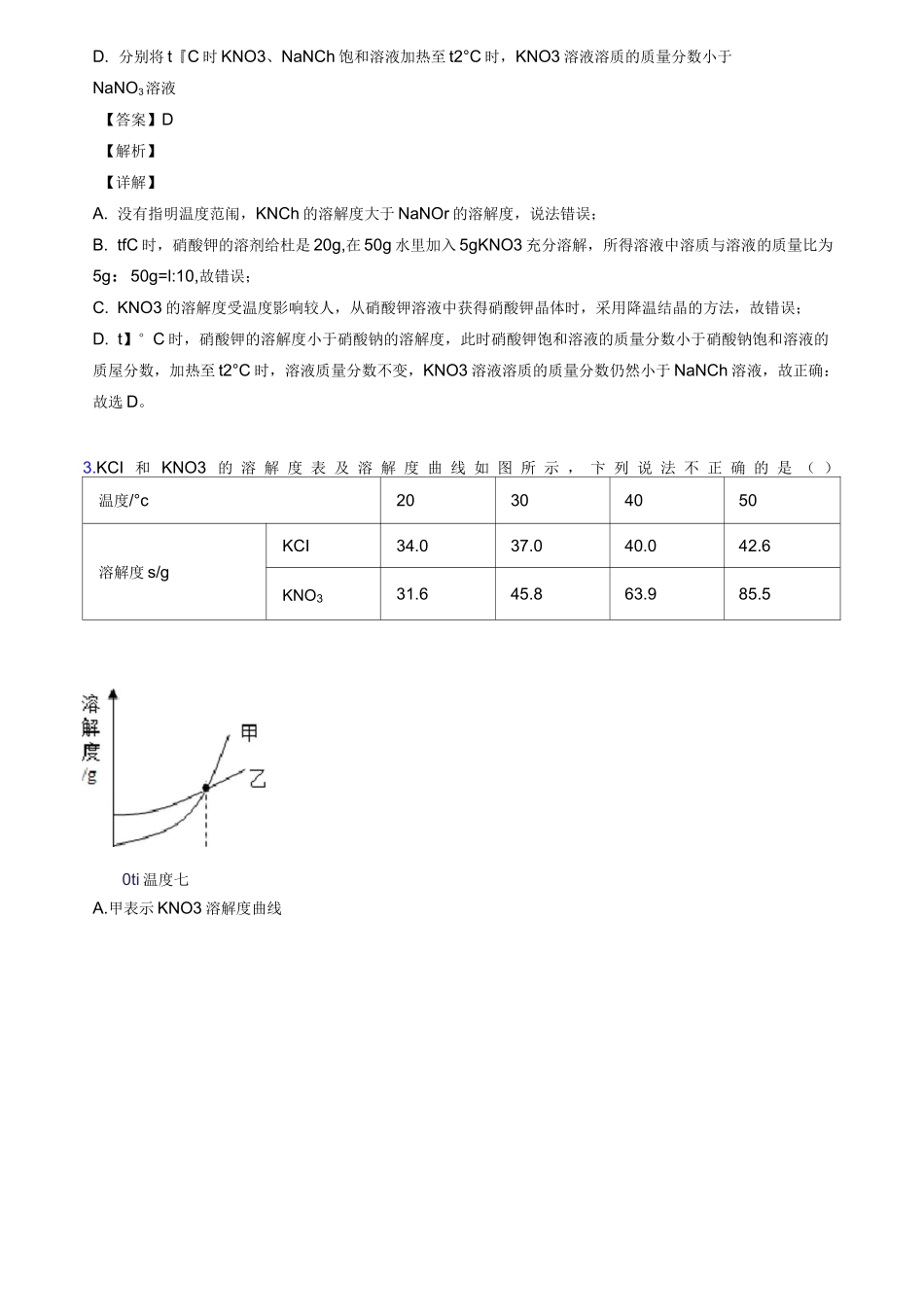
在 t2°C 时,甲、乙两饱和溶液中含的溶质质量一定相等C
甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液D
要从含有少量甲的乙溶液中得到较多的乙晶体,通常可采用降温结晶的方法【答案】A【解析】【分析】从溶解度曲线图看,时,甲、乙、丙的溶解度大小关系为乙>甲>丙,物质甲、乙的溶解度都随温度的升高而增大,丙的溶解度随温度的升高而减少,乙的溶解度随温度的升高变化不大
【详解】A、从溶解度曲线图看,t『C 时,甲、乙、丙的溶解度大小关系:乙>甲>丙,物质甲、乙的溶解度都随温度的升高而增人,所以升温,它们由饱和溶液变为不饱和溶液,但溶液中的溶质和溶剂质屋不变,而丙的溶解度随温度的升高而减少,这样溶质析出,所以所得溶液的溶质质量分数大小顺序是乙>甲>丙,故 A 正确;B、在 t2°C 时,甲、乙的溶解度相等,等质量甲、乙两饱和溶液中含的溶质质量一定相等,故 B 不正确;C、丙的溶解度随温度的升高而减少,故丙物质的饱和溶液升温,会有晶体析出,溶液仍然饱和,故 C 不正确;D、乙的溶解度随温度的升高变化不大,所以要从含有少量甲的乙溶液中得到较多的乙晶体,应采用蒸发结晶的方法,故 D 不正确
【点睛】乙的溶解度随温度的升高变化不人,从含有少量甲的乙溶液中得到较多的乙晶体,采用蒸发结晶的方法
KNCh 和 NaNOs 的溶解度曲线如图所示
卞列说法正确的是()A
KNOs 的溶解度人于 NaNOs 的溶解度B
t『C 时,在 50g 水里加入 5gKNO3 充分溶解,所得溶液中溶质与溶液的质量比为 1:6C
从硝酸钾溶液中获得硝酸钾晶体时,必