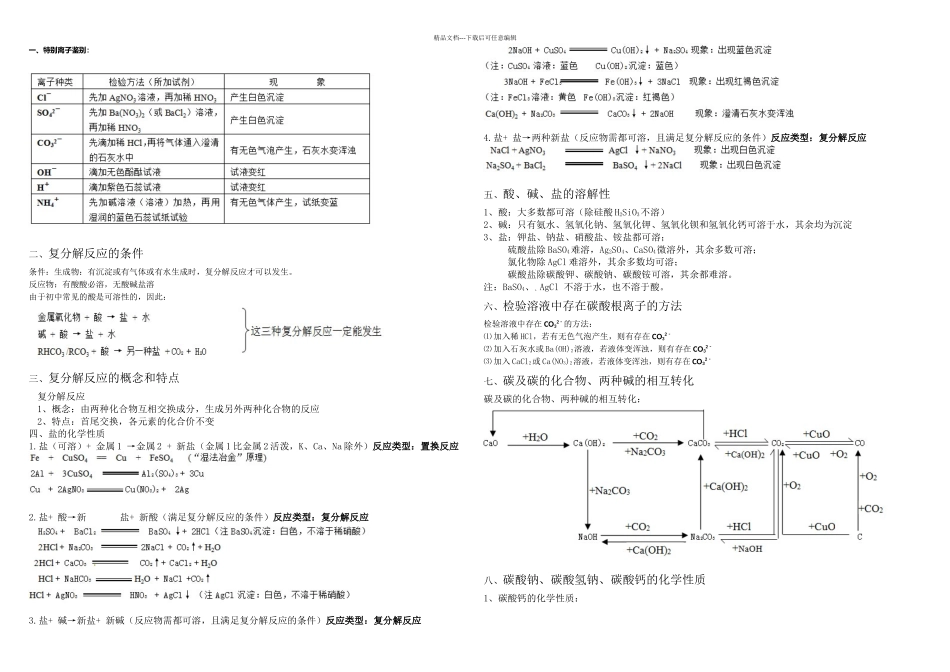
精品文档---下载后可任意编辑一、特别离子鉴别:二、复分解反应的条件条件:生成物:有沉淀或有气体或有水生成时,复分解反应才可以发生
反应物:有酸酸必溶,无酸碱盐溶由于初中常见的酸是可溶性的,因此:三、复分解反应的概念和特点复分解反应1、概念:由两种化合物互相交换成分,生成另外两种化合物的反应2、特点:首尾交换,各元素的化合价不变四、盐的化学性质1
盐(可溶)+ 金属 1 →金属 2 + 新盐(金属 1 比金属 2 活泼,K、Ca、Na 除外)反应类型:置换反应2
盐+ 酸→新盐+ 新酸(满足复分解反应的条件)反应类型:复分解反应3
盐+ 碱→新盐+ 新碱(反应物需都可溶,且满足复分解反应的条件)反应类型:复分解反应4
盐+ 盐→两种新盐(反应物需都可溶,且满足复分解反应的条件)反应类型:复分解反应五、酸、碱、盐的溶解性1、酸:大多数都可溶(除硅酸 H2SiO3不溶)2、碱:只有氨水、氢氧化钠、氢氧化钾、氢氧化钡和氢氧化钙可溶于水,其余均为沉淀3、盐:钾盐、钠盐、硝酸盐、铵盐都可溶;硫酸盐除 BaSO4难溶,Ag2SO4、CaSO4微溶外,其余多数可溶;氯化物除 AgCl 难溶外,其余多数均可溶;碳酸盐除碳酸钾、碳酸钠、碳酸铵可溶,其余都难溶
注:BaSO4、、AgCl 不溶于水,也不溶于酸
六、检验溶液中存在碳酸根离子的方法检验溶液中存在 CO32-的方法:⑴ 加入稀 HCl,若有无色气泡产生,则有存在 CO32-⑵ 加入石灰水或 Ba(OH)2溶液,若液体变浑浊,则有存在 CO32-⑶ 加入 CaCl2或 Ca(NO3)2溶液,若液体变浑浊,则有存在 CO32-七、碳及碳的化合物、两种碱的相互转化碳及碳的化合物、两种碱的相互转化:八、碳酸钠、碳酸氢钠、碳酸钙的化学性质1、碳酸钙的化学性质:精品文档---下载后可任意编辑2、碳酸钠的化学性质:这两个反应可用检验 NaOH 是