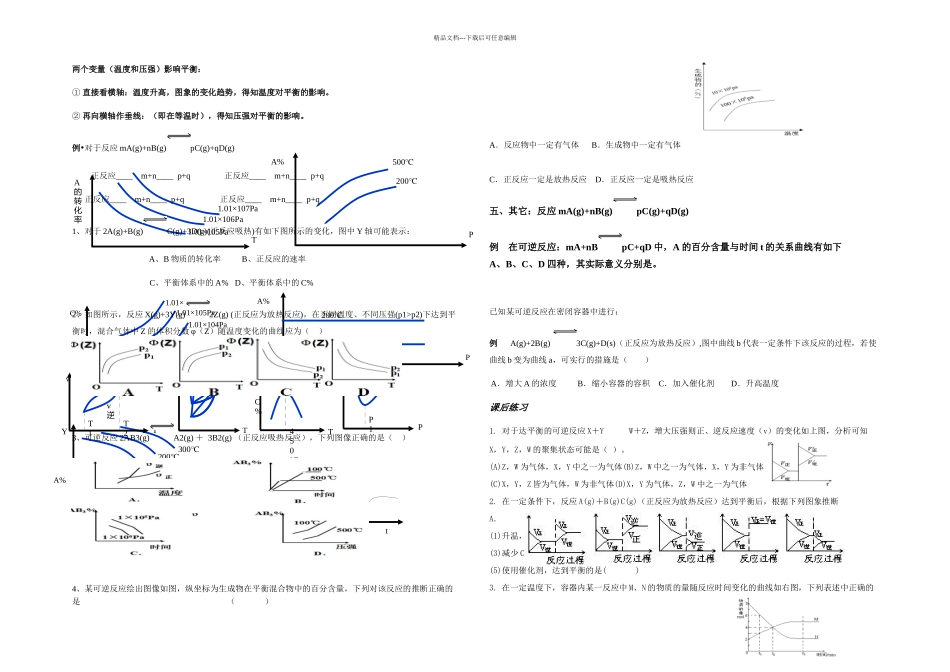
ABCtc43210v逆t1 tvv正DV 正V 逆VtCV 正V 逆VtBV 逆V 正VtAV正V 逆VtV 正V 逆AtVV 逆V 正BVtV正V 逆CVtV 逆V 正DVtv 逆t1 t2tvv正tT1T2A%tA的转化率T1T2tB%T2P2T1P2T1P1TC%1.01*106Pa 1.01*105Pa 1.01*104Pa精品文档---下载后可任意编辑一、、浓度 - 时间图:(化学方程式、化学反应速率、转化1)写出化学反应方程式: 2)求反应物的转化率: 3)vB= VC= 2s 2、可逆反应 H2(g)+I2(g)2HI(g)在一定的条件下反应混合物中各组分的浓度(mol·L-1)与时间 t(min)的变化曲线如图所示,根据图示,回答 (1)时间 t1 的意义是_ . (2)在时间 0 至 t1 的间隔里,v(I2)= . (3)此平衡状态下,H2 的转化率为 . 二、速度-时间图:1) (已知反应)推断引起平衡移动的因素。2)已知引起平衡移动的因素,推断反应是吸热或放热,反应前后气体体积的变化。一点连续、一点突跃是浓度变化对平衡影响的特征。两点跳跃是温度或压强对化学平衡影响的特征。例:右图表示在密闭容器中反应:2SO2+O22SO3+Q 达到平衡时 ,由于条件改变起反应速度和化学平衡的变化情况,ab 过程中改变的条件可能是_;bc 过程中改变的条件可能是_; 若增大压强,反应速度变化情况画在 c—d 处.在密闭容器,一定条件下进行反应,mA(g)+nB(g)pC(g)+qD(g);若增大压强或升高温度,重新达到平衡,变化过程均如图所示,则对该反应叙述正确的是( )A.正反应是吸热反应 B.逆反应是吸热反应 C.m+n>p+qD.m+n
p2 C.T1>T2,p1>p2 D.T1>T2,p1