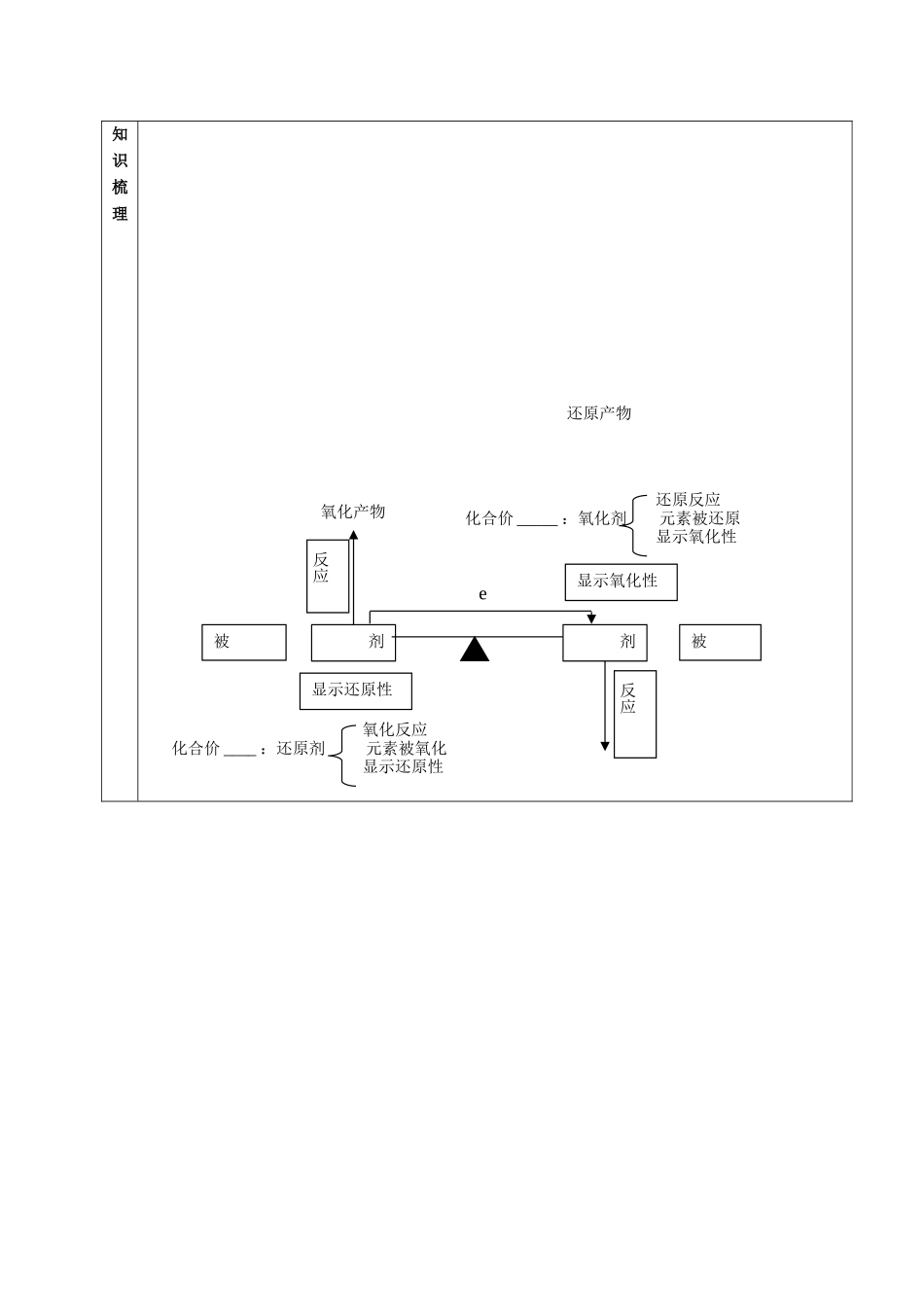
高三化学复习十三氧化还原反应【知识目标】学习内容学习水平氧化还原反应氧化剂与还原剂理解B氧化反应与还原反应理解B氧化还原反应的实质理解B氧化剂硝酸的氧化性理解B过氧化钠的氧化型理解B氧化剂氧化性强弱应用c还原剂钠的还原性理解B还原剂还原性强弱应用c氧化还原反应方程式的配平化合价升降法配平方程式应用c知识点1、四组概念辨析知识梳理还原反应化合价_____:氧化剂元素被还原显示氧化性剂氧化产物剂e反应反应被被显示氧化性显示还原性氧化反应化合价____:还原剂元素被氧化显示还原性还原产物概念定义要点氧化还原反应有电子转移(得失或共用电子对的偏移)的反应电子转移是本质,化合价的升降是标志氧化反应物质所含元素化合价升高的反应物质所含元素的原子失去电子的外部表现为元素化合价的升高还原反应物质所含元素化合物价降低的反应物质所含元素的原子得到电子的外部表现为元素化合价的降低被氧化元素失去电子的过程物质发生了氧化反应,这一变化可称为被氧化被还原元素得到电子的过程物质发生了还原反应,这一变化可称为被还原氧化剂得到电子的反应物氧化剂在反应中被还原。常见氧化剂:活泼的非金属单质、高价金属阳离子、高价或较高价含氧化合物、过氧化物还原剂失去电子的反应物还原剂在反应中被氧化。常见还原剂:活泼或较活泼的金属、一些非金属单质、较低价态的化合物氧化性得到电子的能力物质的氧化性、还原性的强弱与其得失电子能力有关,与得失电子数目无关。还原性失去电子的能力【例1】下列类型的反应,一定发生电子转移的是A.化合反应B.分解反应C.置换反应D.复分解反应【例2】下列物质中,按只有氧化性,只有还原性,既有氧化性又有还原性的顺序排列的一组是A.F2、K、HClB.Cl2、Al、H2C.NO2、Na、Br2D.O2、SO2、H2O【例3】下列说法中错误的是A.凡是氧化还原反应,都不可能是复分解反应B.化合反应不可能是氧化还原反应C.置换反应一定是氧化还原反应D.分解反应可能是氧化还原反应【例4】下面有关氧化还原反应的叙述不正确的是A.在反应中不一定所有元素的化合价都发生变化B.肯定有一种元素被氧化,另一种元素被还原C.在氧化还原反应中,失去电子的物质,所含元素化合价升高D.氧化还原反应的本质是电子的转移【例5】实验室利用氧化还原反应制取的气体是A.O2H2CO2B.O2CO2C.H2O2D.CO2【例6】CaH2常做生氢剂,其中氢元素是-1价,化学方程式为:CaH2+2H2O→Ca(OH)2+2H2↑,其中水是A.还原剂B.既是氧化剂,又是还原剂C.氧化剂D.既不是氧化剂,又不是还原剂知识点2、三个原理应用△知识梳理1、得失电子守恒。氧化还原反应发生,元素化合价有升必有降。氧化剂得到电子总数=还原剂失去电子总数。2、归中不交叉。对于同一种元素不同价态之间发生的氧化还原反应,就化合价来说,高价的降低,低价的升高,升降后最大程度只能相等,绝不能交叉。3、强弱规律。①理论判断“一表二序”:元素周期表、金属活动顺序、非金属活动顺序②事实判断“化学反应”:a.根据化学反应的“方向”判断。Cl2+2KBr→2KCl+Br2氧化性:Cl2>Br2,b.根据化学反应的“程度”判断。Cu+Cl2→CuCl2;2Cu+S→Cu2S氧化性:Cl2>Sc.根据化学反应的“难易”判断。4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O16HCl+2KMnO4→2KCl+2MnCl2+5Cl2↑+8H2O【例1】某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。(1)已知KBrO3在反应中得到电子,则该反应的还原剂是。(2)已知0.2molKBrO3在反应中得到1mol电子生成X,则X的化学式为。【例2】24毫升浓度为0.05摩/升的Na2SO3溶液,恰好与20毫升浓度为0.02摩/升的K2Cr2O7溶液完全反应,则元素Cr在被还原的产物中的化合价是A.+6B.+3C.+2D.0【例3】以下关于化学反应KClO3+6HCl→KCl+3Cl2↑+3H2O中,电子转移的方向和数目的叙述中,正确的是A.Cl由-1价升高到0价失去6e-B.Cl由+5价降低到0价得到5e-C.Cl由+5价降低到-1价得到6e-D.以上反应不是氧化还原反应【例4】在下图所表示的微粒中,氧化性最强的是ABCD【例5】在常温下,发生下列几种反应:①16H++10Z-+2XO4-→2X2++5Z2+8H2O;②2A2++B2...