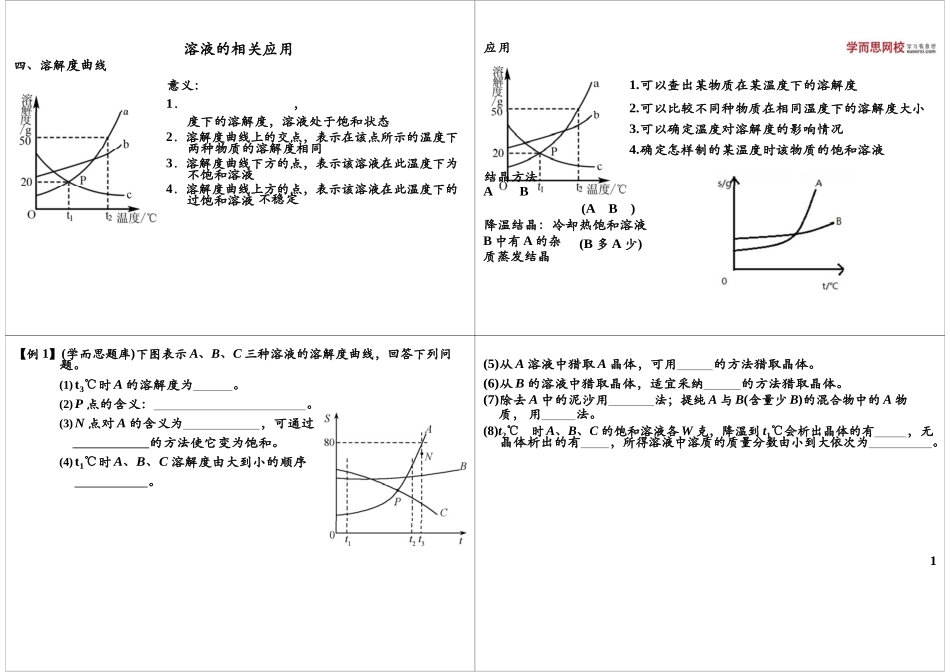
四、溶解度曲线溶液的相关应用意义:1.,度下的溶解度,溶液处于饱和状态2.溶解度曲线上的交点,表示在该点所示的温度下两种物质的溶解度相同3.溶解度曲线下方的点,表示该溶液在此温度下为不饱和溶液4.溶解度曲线上方的点,表示该溶液在此温度下的过饱和溶液 不稳定应用结晶方法AB1
可以查出某物质在某温度下的溶解度2
可以比较不同种物质在相同温度下的溶解度大小3
可以确定温度对溶解度的影响情况4
确定怎样制的某温度时该物质的饱和溶液(AB)降温结晶:冷却热饱和溶液B 中有 A 的杂质蒸发结晶(B 多 A 少)【例 1】(学而思题库)下图表示 A、B、C 三种溶液的溶解度曲线,回答下列问题
(1)t3℃时 A 的溶解度为
(2)P 点的含义:
(3)N 点对 A 的含义为 ,可通过 的方法使它变为饱和
(4)t1℃时 A、B、C 溶解度由大到小的顺序
(5)从 A 溶液中猎取 A 晶体,可用 的方法猎取晶体
(6)从 B 的溶液中猎取晶体,适宜采纳 的方法猎取晶体
(7)除去 A 中的泥沙用 法;提纯 A 与 B(含量少 B)的混合物中的 A 物质, 用 法
(8)t2℃ 时 A、B、C 的饱和溶液各 W 克,降温到 t1℃会析出晶体的有 ,无晶体析出的有 ,所得溶液中溶质的质量分数由小到大依次为
1五、溶液组成的表示方法(2)浓溶液稀释稀释前后溶质质量不变m 溶质1.溶质的质量分数 =溶液m 溶质=×100%×100%欲配制 500g 质量分数为 20% 的稀 H2SO4,需要质量分数为 80%的浓 H2SO4多少克
需加水多少克
【例 1】 2
8g 铁放入 73g 质量分数为 10%的稀 HCl 中,充分反应,求反应m 溶质 + m 溶剂相同温度下,同种物质的饱和溶液质量分数相等2.溶液的配制(1)用固体物质配制如何配制 100g 质量分数为 15% 的 NaCl 溶液