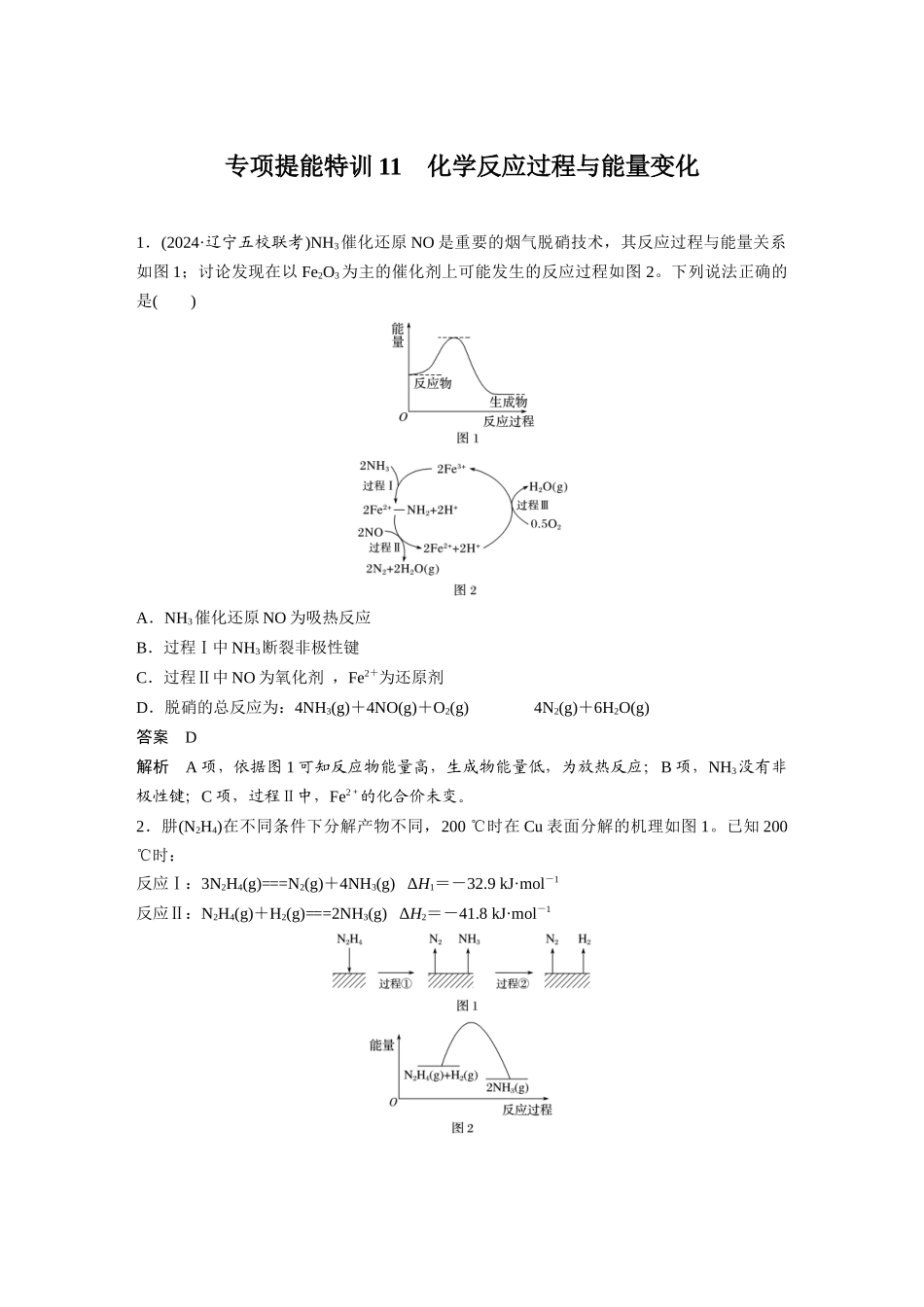
专项提能特训 11 化学反应过程与能量变化1.(2024·辽宁五校联考)NH3催化还原 NO 是重要的烟气脱硝技术,其反应过程与能量关系如图 1;讨论发现在以 Fe2O3为主的催化剂上可能发生的反应过程如图 2
下列说法正确的是( )A.NH3催化还原 NO 为吸热反应B.过程Ⅰ中 NH3断裂非极性键C.过程Ⅱ中 NO 为氧化剂 ,Fe2+为还原剂D.脱硝的总反应为:4NH3(g)+4NO(g)+O2(g)4N2(g)+6H2O(g)答案 D解析 A 项,依据图 1 可知反应物能量高,生成物能量低,为放热反应;B 项,NH3没有非极性键;C 项,过程Ⅱ中,Fe2+的化合价未变
2.肼(N2H4)在不同条件下分解产物不同,200 ℃时在 Cu 表面分解的机理如图 1
已知 200 ℃时:反应Ⅰ:3N2H4(g)===N2(g)+4NH3(g) ΔH1=-32
9 kJ·mol-1反应Ⅱ:N2H4(g)+H2(g)===2NH3(g) ΔH2=-41
8 kJ·mol-1下列说法不正确的是( )A.图 1 所示过程①是放热反应、②是吸热反应B.反应Ⅱ的能量过程示意图如图 2 所示C.断开 3 mol N2H4(g)中的化学键吸收的能量大于形成 1 mol N2(g)和 4 mol NH3(g)中的化学键释放的能量D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为 N2H4(g)===N2(g)+2H2 (g) ΔH=+50
7 kJ·mol-1答案 C解析 图 1 所示过程①发生的反应是Ⅰ,为放热反应,过程②是 NH3(g)的分解,是吸热反应,A 正确;反应Ⅱ是放热反应,图 2 所示的能量过程示意图正确,B 正确;由于反应Ⅰ为放热反应,因此断开 3 mol N2H4(g)中的化学键吸收的能量小于形成 1 mol N2(g)和 4 mol NH3(g)中的化学键释放的