化学能与电能(学案一)【学习目标】1.了解化学能与电能的转化关系
2.初步了解化学电池的工作原理及应用
3.了解研制新型电池的重要性
4.会书写简单的电极反应式和电池反应式
【目标一】火电(间接转变)1.我国目前发电总量构成:火电----81
2% 水电----17
6% 其他----1
2%(今后水电和其他发电量会逐步增加)
2.火力发电原理:通过化石燃料燃烧,使化学能转变为热能,加热使水汽化为蒸汽以推动蒸汽轮机,然后带动发电机发电
`3.火力发电流程:(学生回答)4.火力发电缺点:①转换环节多;②发电效率低;③能源浪费多;④环境污染严重等
5.燃烧的氧化还原反应本质:(学生回答)氧化剂与还原剂之间发生电子转移,引起化学键重新组合,伴随有能量变化
【思考】能否将化学能直接转化为电能呢
【目标二】原电池原理1.概念:将 的装置
从理论上讲,能自发进行的氧化还原反应(即符合强氧化剂与强还原剂反应生成弱的氧化剂与弱的还原剂的反应),都可设计为原电池
2.原电池正、负极概念:以 Zn|H2SO4|Cu 原电池为例,如下图所示:稀硫酸负极(Zn): (氧化反应)正极(Cu): (还原反应)总反应: (氧化还原反应)负极:较活泼的一极或电子流出的极,发生氧化反应的极
正极:较不活泼的一极或电子流入的极,发生还原反应的极
3.构成原电池的条件:【实验探究】探究原电池构成条件实验一:【归纳小结】形成条件一:活泼性不同的两个电极
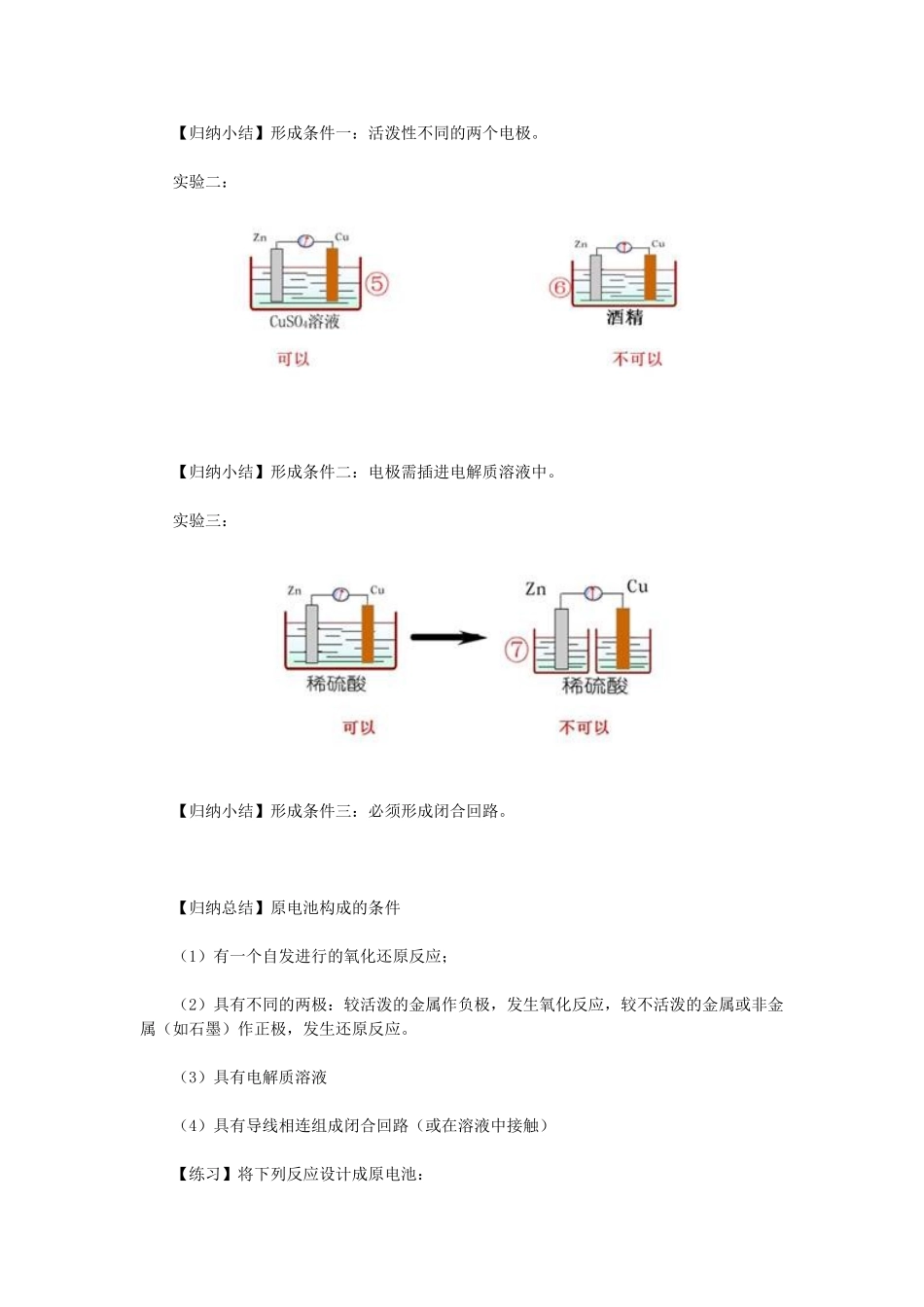
实验二: 【归纳小结】形成条件二:电极需插进电解质溶液中
实验三:【归纳小结】形成条件三:必须形成闭合回路
【归纳总结】原电池构成的条件(1)有一个自发进行的氧化还原反应;(2)具有不同的两极:较活泼的金属作负极,发生氧化反应,较不活泼的金属或非金属(如石墨)作正极,发生还原反应
(3)具有电解质溶液(4)具有导线相连组成闭合回路(或在溶液中接触)【练习】将下列