化学变化中的能量变化一、教学目标知识目标:1、掌握吸热、放热反应的概念,理解反应热的含义
2、理解热化学方程式的意义,能正确推断热化学方程式
3、应用反应热的数据,推断反应物和生成物之间能量变化及化合物反应中生成物的热稳定性
情感目标:1、创设学生自主学习、互助学习的氛围
2、树立起能源节约的意识,养成环保的理念
技能目标:培育学生的实验观察能力,培育学生阅读、分析、推理等学习能力
二、重点和难点1
反应热的含义和应用,热化学方程式的意义
应用反应热理解化学反应中的能量变化
三、教学过程引入: 世界是物质的,物质会发生变化
物质的变化总是和能量变化联系在一起,而能量变化通常以热量变化表现出来
物质的变化分为物理变化和化学变化
化学变化中的能量变化要远大物理变化中的能量变化
[引入]1、相关材料阅读和分析
2、演示实验: 1)、不用火柴点燃酒精灯 2)、锌和碘反应 3)、原电池反应化学变化中有能量释放出来,形式有光能、电能、热能等,其中以热能最多见
[板书] 4
2 化学变化中的能量变化 一 、化学反应中的热现象1、反应的热效应:化学变化中普遍伴随着能量变化
反应中放出或吸收的热量叫做反应的热效应
2、反应热效应的表示 “放热反应用 +Q”表示 “吸热反应用 -Q”表示3、放热反应和吸热反应4、反应热可以用实验方法测定[过渡]:我们把反应中放出或吸收的热量直接写入化学方程式,用来表示化学反应中的热效应,这种方程式叫做热化学方程式
[讨论]:热化学方程式与化学方程式的不同点2H2+O2点燃 2H2O 2H2(g)+O2(g) → 2H2O(l)+571
6KJ 2H2(g)+O2(g) → 2H2O(g)+483
6KJ H2(g)+1/2O2(g)→ H2O(g)+241
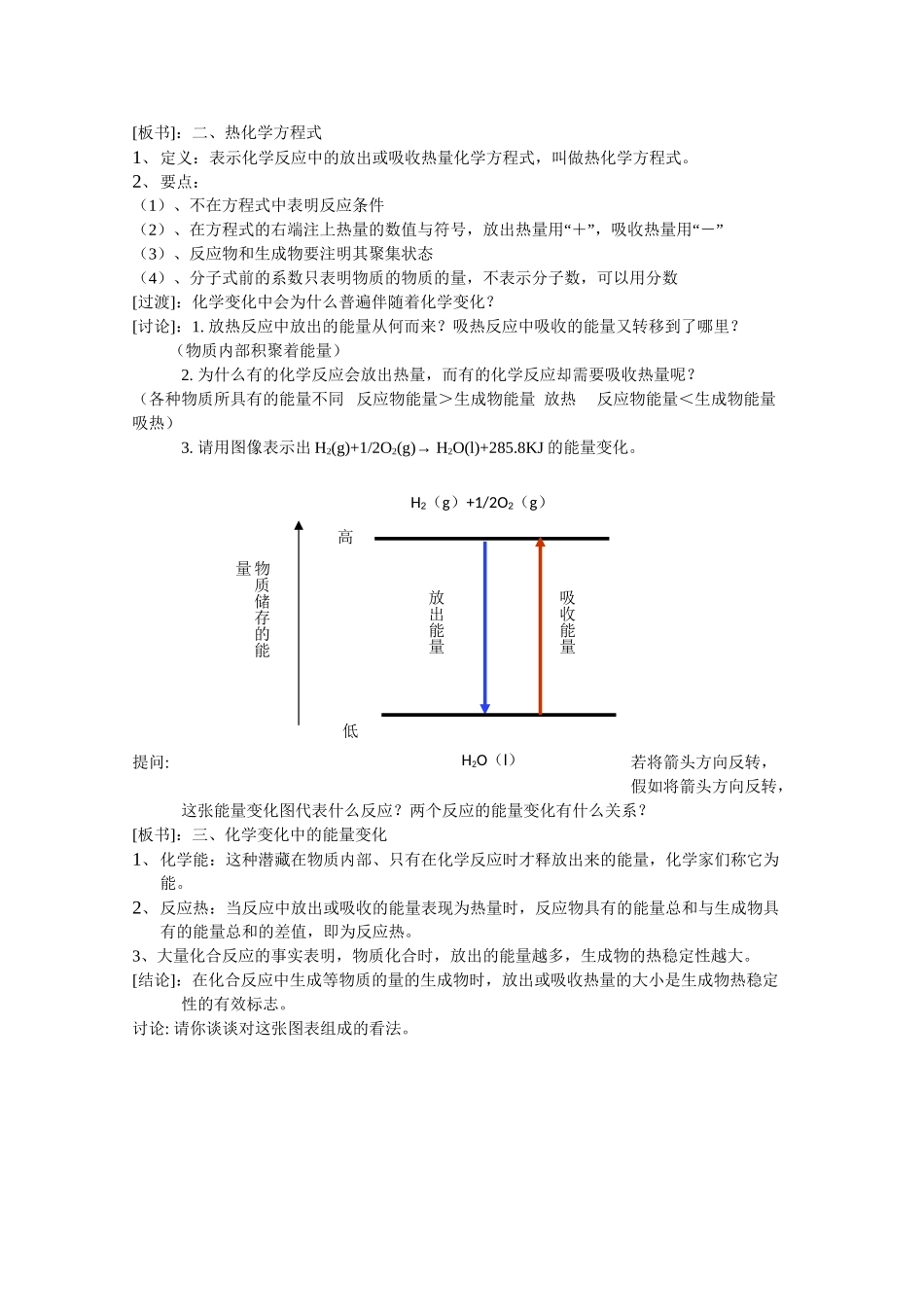
8KJ[板书]:二、热化学方程式1、定义:表示化学反应中的放出或吸收热量化学方程式,叫做热