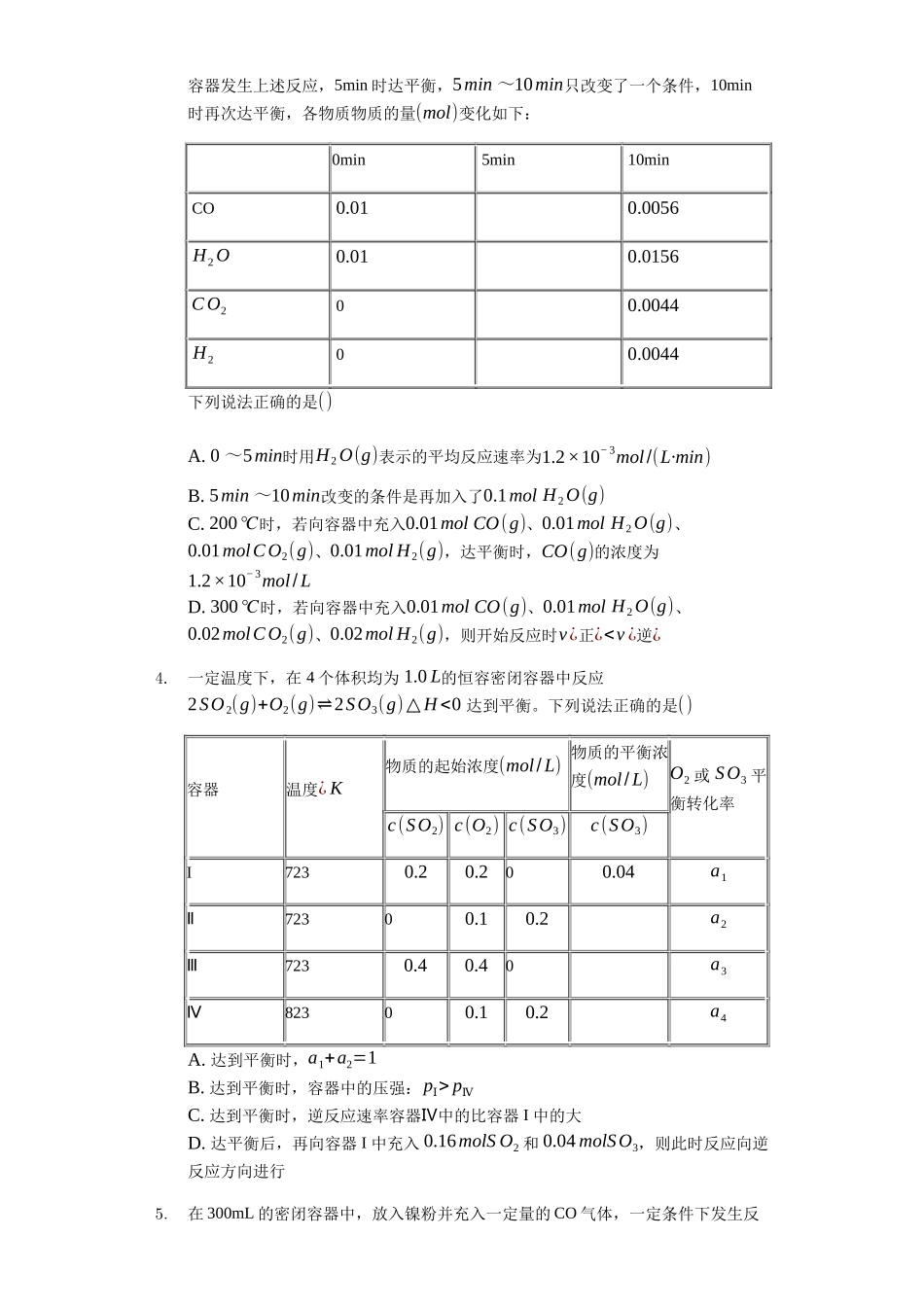
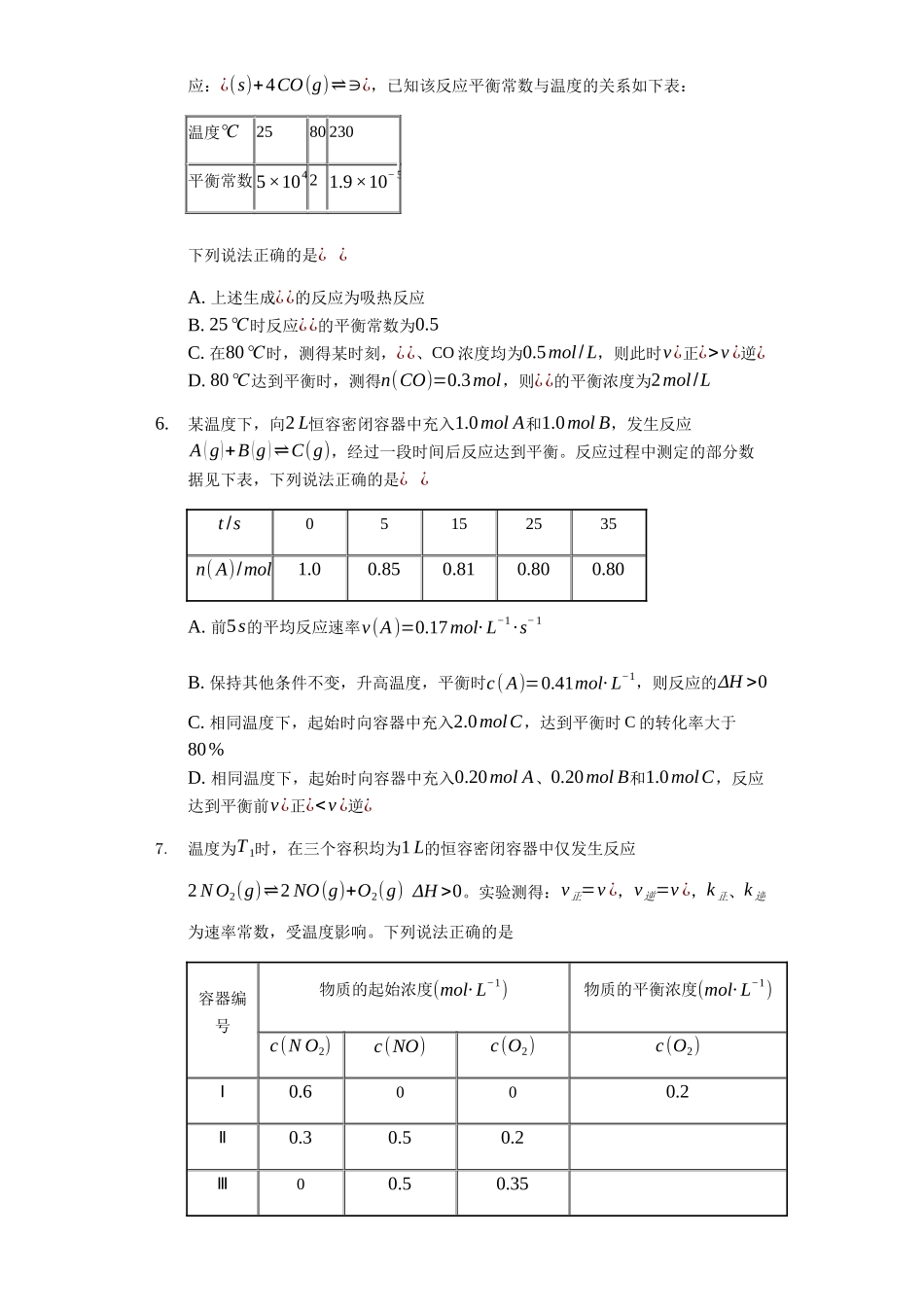
届高三化学二轮冲刺——浓度商与化学平衡常数的关系选择专练【能力提升20题】1
一定温度下,在三个体积均为1
0L恒容密闭容器中发生反应:下列说法正确的是()窗口编号温度(℃)起始物质的量(mol)平衡物质的量(mol)H2(g)13800
06023800
2032300
该反应的正反应为放热反应B
达到平衡时,容器1中的H2体积分数比容器2中的小C
容器1中反应达到平衡所需的时间比容器3中的长D
若起始时向容器Ⅲ中充入0
10mol(g)、0
10mol(g)和0
10molH2,则反应向逆反应方向进行2
在密闭容器中有可逆反应:nA(g)+mB(g)⇌pC(g);ΔH>0处于平衡状态¿已知m+n>p¿,则下列说法正确的是()①升温时c(B)c(C)的值减小②降压时体系内混合气体的平均相对分子质量减小③加入B,A的转化率变大④加入催化剂,气体的总物质的量不变⑤充入C,则A、B的物质的量增大A
有反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H0C
相同温度下,起始时向容器中充入2
0molC,达到平衡时C的转化率大于80%D
相同温度下,起始时向容器中充入0
20molA、0
20molB和1
0molC,反应达到平衡前v¿正¿0
实验测得:v正=v¿,v逆=v¿,k正、k逆为速率常数,受温度影响
下列说法正确的是容器编号物质的起始浓度(mol·L−1)物质的平衡浓度(mol·L−1)c(NO2)c(NO)c(O2)c(O2)Ⅰ0
反应达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为1:1B
反应达平衡时,容器Ⅱ中c(O2)c(NO2)比容器Ⅰ中的大C
反应达平衡时,容器Ⅲ中NO的体积分数大于50%D
当温度改变为T2时,若k正=k逆,