中考总复习:质量守恒定律和化学方程式(提高)【考纲要求】1.了解质量守恒定律的内容,能从宏观和微观上理解并运用“六不变、两变、两可能变”
2.了解化学方程式的含义、读法及各物质间的质量关系;掌握化学方程式的书写步骤、原则及配平化学方程式的方法
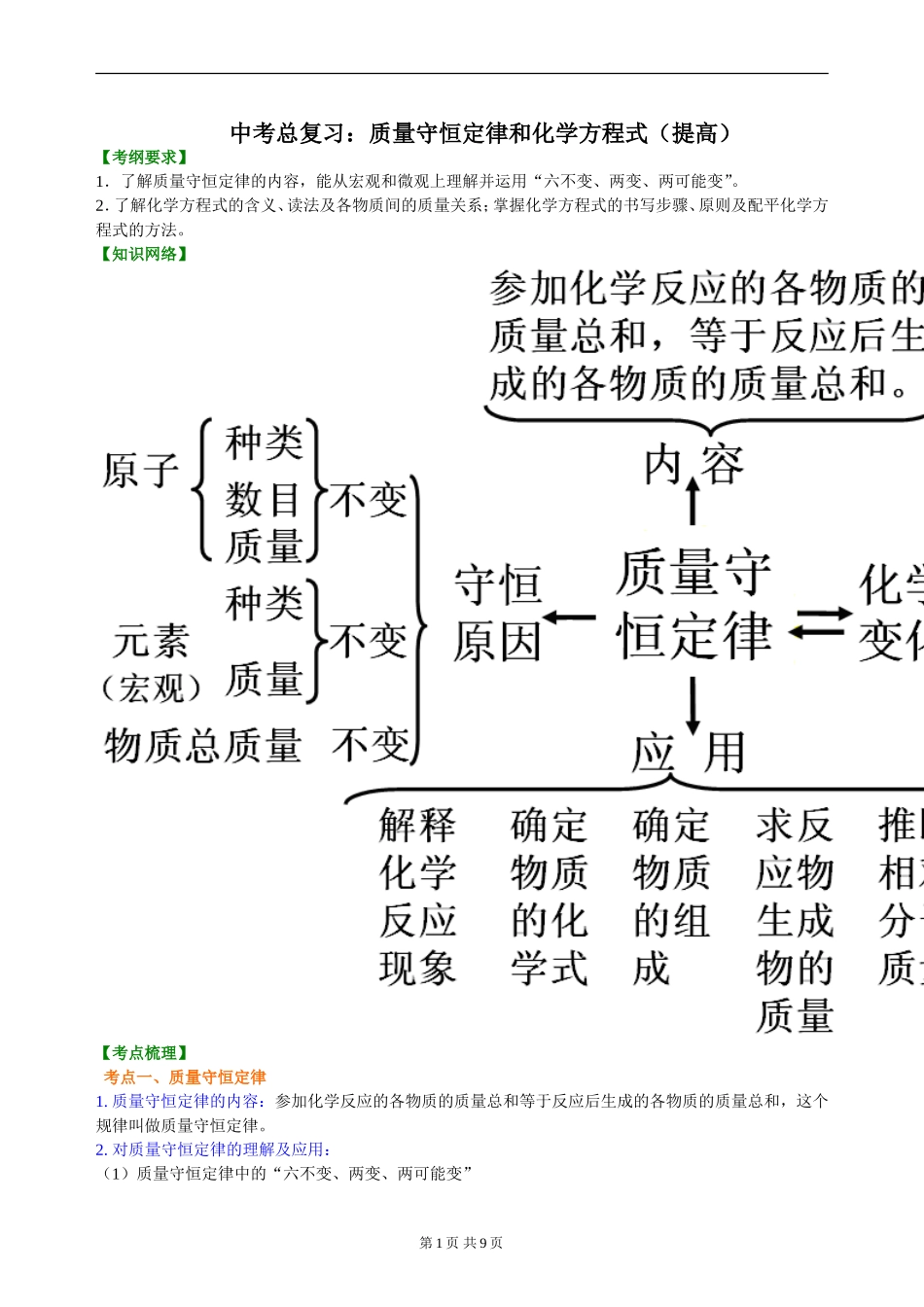
【知识网络】 【考点梳理】考点一、质量守恒定律1
质量守恒定律的内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,这个规律叫做质量守恒定律
对质量守恒定律的理解及应用: (1)质量守恒定律中的“六不变、两变、两可能变”第 1 页 共 9 页 参与反应的反应物和生成物的总质量不变 宏观 元素的种类不变 元素的质量不变六个不变 原子的种类不变微观 原子的数目不变 原子的质量不变 宏观:物质的种类一定改变两个一定改变 微观:分子的种类一定改变可能改变:分子总数可能改变;元素的化合价
(2)质量守恒定律的微观解释:化学反应的实质是分子的破裂和原子的重新组合
在化学反应中,由于只是发生了原子间的重新组合,原子的种类和数目并没有发生变化,原子的质量也没有发生变化,所以,反应前后各物质的质量总和必然相等
(3)质量守恒定律的应用 ①解释常见化学现象中的质量关系,如:铁生锈质量增加,木炭燃烧成灰质量减少等
②利用质量守恒定律,根据化学方程式确定物质的化学式; ③利用质量守恒定律,根据化学方程式确定物质的相对分子质量; ④熟练进行化学方程式的配平;根据题中所给的信息,利用质量守恒定律写出未学过的化学反应方 程式;根据化学方程式求某元素质量; ⑤利用质量守恒定律,根据化学方程式求反应中某物质的质量; ⑥结合化学方程式中各物质的质量比,判断某反应物是否全部参加了反应……【要点诠释】1
质量守恒定律内容的剖析(1)前提条件:化学反应中
(2)研究对象:所有参加反应和生成的物质
(不论状态:气体、液体、固体)(3)研究内容:质量