化学中常用物理量——物质的量【学习目标】 1、了解摩尔、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数等的含义2、根据物质的量与微粒(原子、分子、离子等)数目、气体体积(标况下)之间的相互关系进行有关的计算
3、了解配制一定溶质质量分数、物质的量浓度溶液的方法
【使用说明】 利用一节课,认真阅读课本完成学案,下课收齐
下节课修改 10 分钟后结合错题统计讨论 10 分钟,师生探究、学生展示 20 分钟,巩固落实 5 分钟
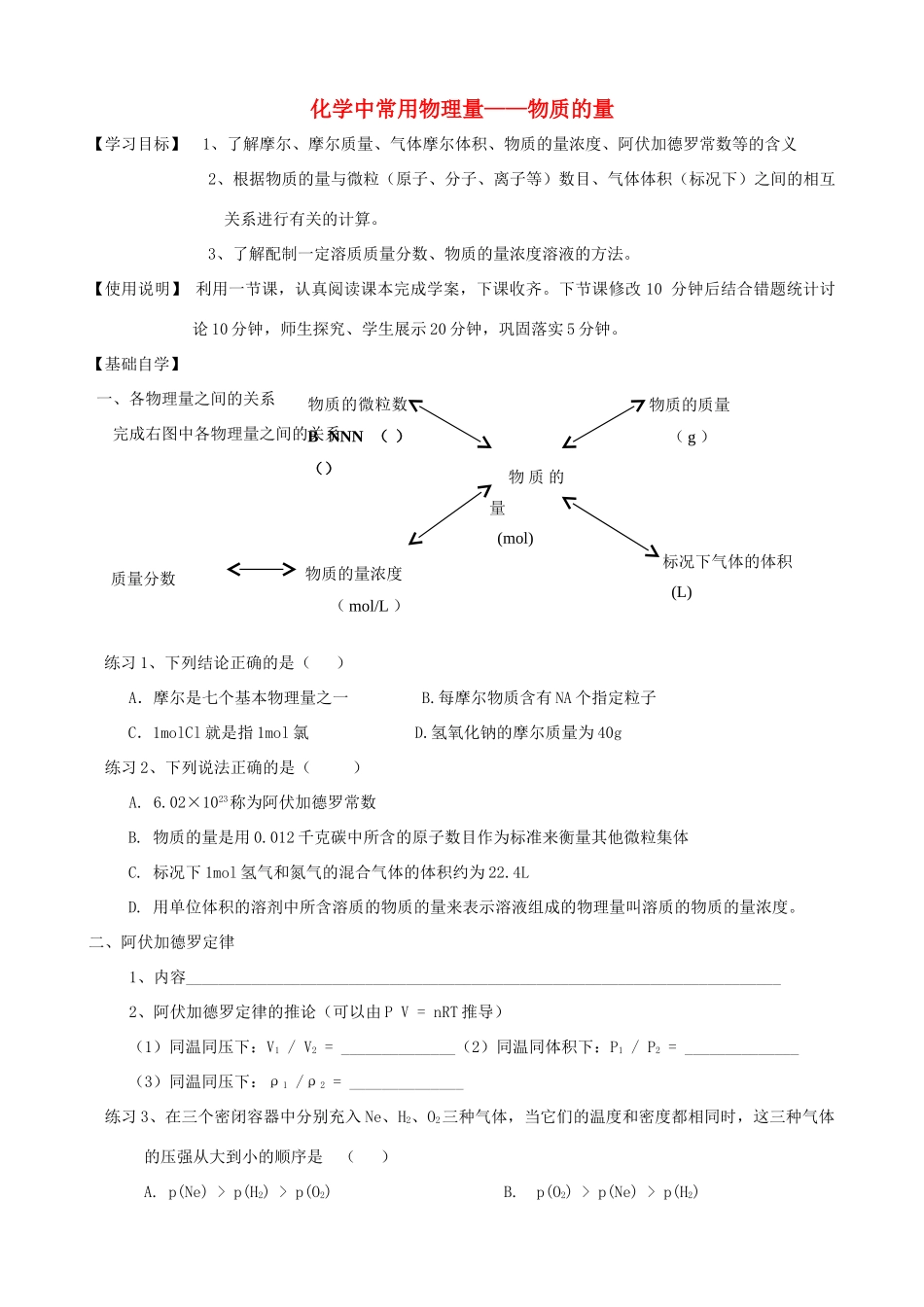
【基础自学】 一、各物理量之间的关系 完成右图中各物理量之间的关系 练习 1、下列结论正确的是( ) A.摩尔是七个基本物理量之一 B
每摩尔物质含有 NA 个指定粒子C.1molCl 就是指 1mol 氯 D
氢氧化钠的摩尔质量为 40g 练习 2、下列说法正确的是( ) A
02×1023称为阿伏加德罗常数B
物质的量是用 0
012 千克碳中所含的原子数目作为标准来衡量其他微粒集体C
标况下 1mol 氢气和氮气的混合气体的体积约为 22
用单位体积的溶剂中所含溶质的物质的量来表示溶液组成的物理量叫溶质的物质的量浓度
二、阿伏加德罗定律 1、内容_________________________________________________________________________ 2、阿伏加德罗定律的推论(可以由 P V = nRT 推导)(1)同温同压下:V1 / V2 = ______________(2)同温同体积下:P1 / P2 = ______________(3)同温同压下:ρ1 /ρ2 = ______________练习 3、在三个密闭容器中分别充入 Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强从大到小的顺序是 ( )A
p(Ne) > p(H2) > p(O2) B