江苏省 2013-2014 学年高中化学 专题三 1
2 铝的氧化物与铝的氢氧化物同步导学案 苏教版必修 1一:学习目标1、 掌握 Al2O3和 Al(OH)3的两性,特别是要会书写与强碱反应的方程式;2、 能根据 Al2O3和 Al(OH)3的有关性质进行除杂和鉴别;3、 理解 Al(OH)3的制备所需试剂:4、 熟练掌握“铝四方”的基础之上,掌握从铝土矿中提取铝的基本流程及有关反应
二:课前预习(一)、Al2O31. 存在:铝土矿、刚玉、红宝石、蓝宝石
2. 物理性质:难溶;难熔;高硬度3
化学性质:既能与酸反应,又能与强碱反应 (1)与酸反应的化学方程式: 学生改写离子方程式: (2)与强碱反应的化学方程式: 学生改写离子方程式: 结论:两性氧化物:既能与酸反应,又能与碱反应生成盐和水的氧化物(二)、Al(OH)31、制取:通常选用的试剂是:可溶性铝盐和氨水 写出氯化铝和氨水反应的化学方程式和离子方程式: 2、NaAlO2的性质:类别: 水溶性: 基本化学性质: (1)向偏铝酸钠溶液中通入二氧化碳能否反应
写出反应的方程式
并写出相应的离子方程式
通入少量的二氧化碳: 通入过量的二氧化碳: 三.课堂研讨 1.引导学生回忆:什么是酸性氧化物
什么是碱性氧化物
用方程式加以说明
酸性氧化物: 碱性氧化物: 问题讨论:如何除去氧化铁中的氧化铝
2、请你思考,为什么 Al(OH)3的制备,所选的碱不用强碱(如 NaOH 等),而用弱碱氨水呢
原因分析:(实验及有关方程式); 结论:Al(OH)3既能与酸反应,又能与强碱反应,因此 Al(OH)3也具有两性,我们把它叫做两性氢氧化物
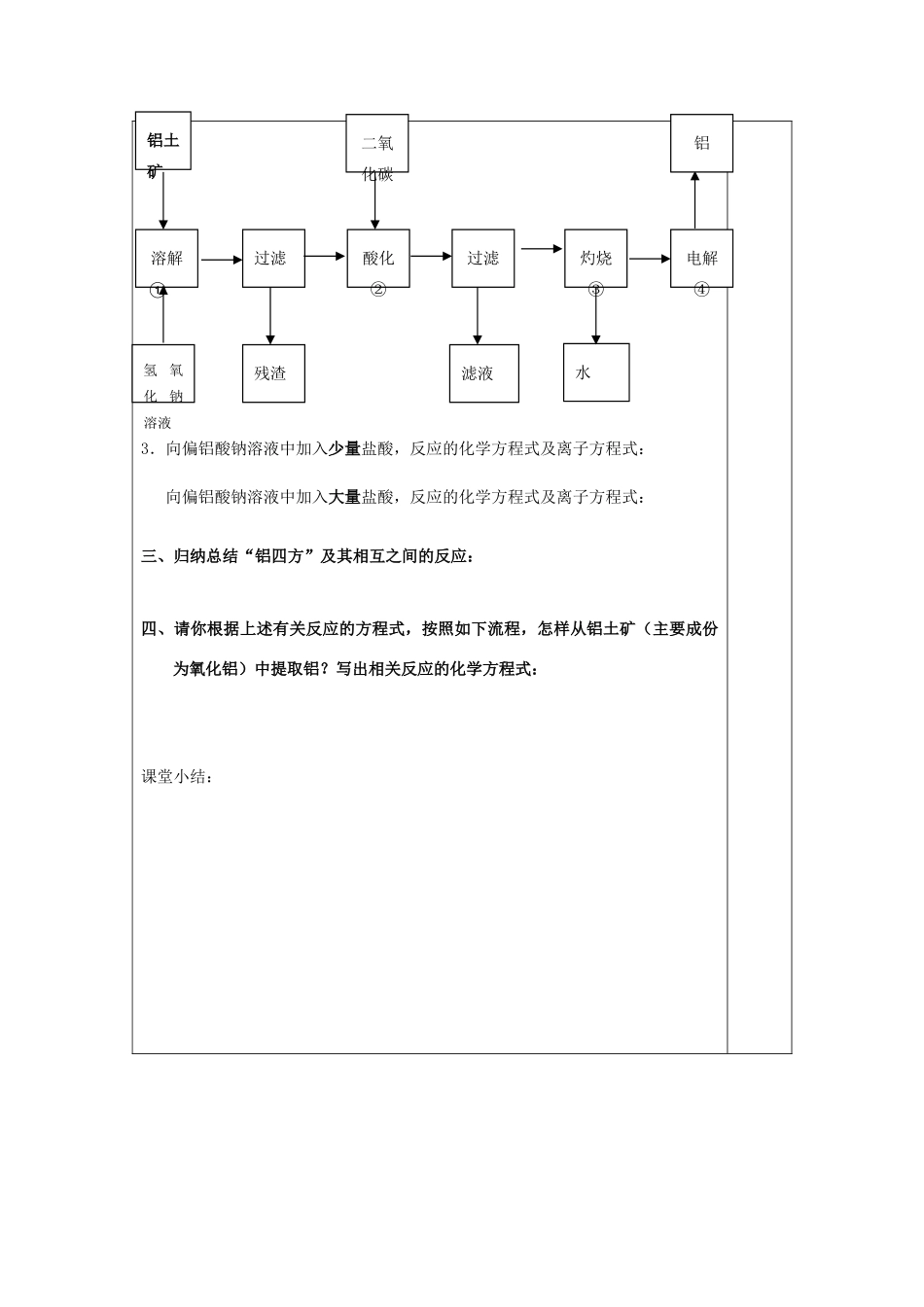
备注3.向偏铝酸钠溶液中加入少量盐酸,反应的化学方程式及离子方程式: 向偏铝酸钠溶液中加入大量盐酸,反应的化学方程式及离子方程式: 三、归纳总结“铝四方”及其相互之间的反应:四、请你根据上述有