江苏省 2013-2014 学年高中化学 专题三 1
3 从铝地矿中提取铝同步导学案 苏教版必修 1一:学习目标1、了解铝在地壳中金属元素的含量;2、了解铝元素在自然界中的主要存在形式;了解工业上获得铝的方法
3、从金属铝的冶炼方法的变化体验化学科学的发展对人类生活的影响
二:课前预习1.铝元素占地壳总量的 ,是地壳中含量 最多 的金属元素
铝土矿(主要成分为 ,还有少量的 、 等杂质)是铝元素在地 壳中的主要存在形式之一,要从铝土矿中提取铝,必须获得纯度较高的 用于电解
2.从铝土矿中提出 Al2O3 的两种方法 方法一:方法二:3.金属铝呈 色,硬度 ,密度 ,熔点 ,和镁类似,铝的主要用途是制造铝合金,铝优良的导电性和密度小,使铝大量用来制作导线
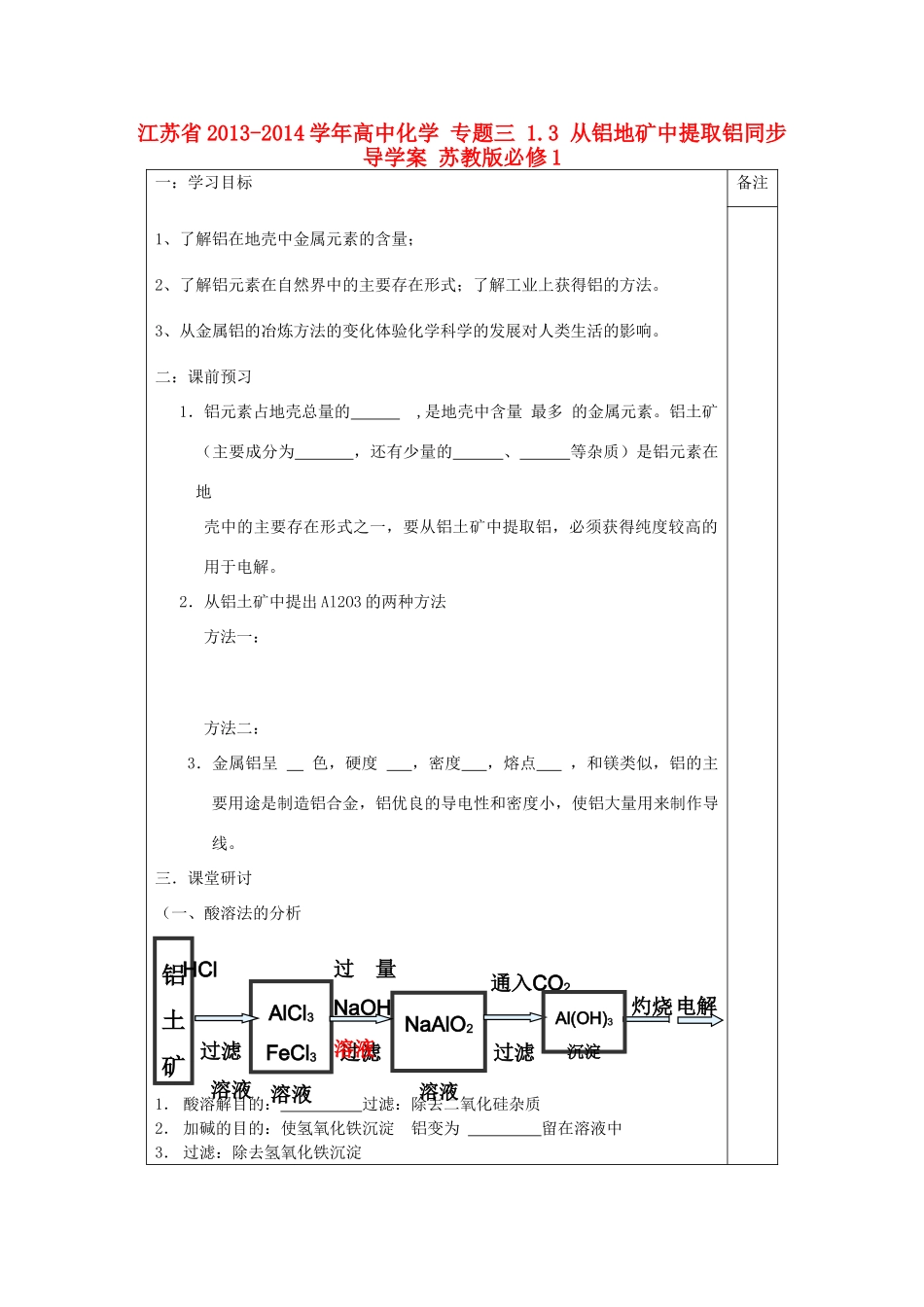
三.课堂研讨 (一、酸溶法的分析1. 酸溶解目的: 过滤:除去二氧化硅杂质2. 加碱的目的:使氢氧化铁沉淀 铝变为 留在溶液中3. 过滤:除去氢氧化铁沉淀备注铝土矿AlCl3FeCl3溶液NaAlO2溶液HCl 溶液过滤灼烧电解通入CO2过量NaOH溶液过滤Al(OH)3沉淀过滤4. 通入 CO2酸化的目的:NaAlO2+CO2+2H2O=Al(OH)3↓ +NaHCO 3反应原理:强酸制备弱酸思考能否用更强的酸 HCl 溶液来制备 Al(OH)3教师实验:NaAlO2溶液中通入足量 CO2 NaAlO2溶液中逐滴滴加稀 HCl 溶液学生:观察现象,解释现象;书写方程式;摄像展示结果教师归纳:足量 CO2使 Al(OH)3完全沉淀;若用盐酸难控制用量,经济上不节约
6.过滤:获得氢氧化铝沉淀7.灼烧: 8.电解:教师:讲解,其实氧化铝的熔点很高大约是两千摄氏度,直到 1886 年霍尔在氧化铝中加入了一种叫做冰晶石(Na3AlF6)的物质,才使得氧化铝的熔融温度大大的降低下来,使得电解法制铝工艺能够成功的得以实现