江苏省响水中学 2014 高中化学《第 13 课 氯气的生产原理 》教学案 新人教版必修 1教学目标:1
掌握氯气的生产原理
通过分析实验现象,增强发现问题和解决问题的能力
通过学习,认识到海水是人类宝贵的自然资源,培养与大自然友好相处的情感
教学重难点:氯气的生产原理教学过程:【激趣导学】1
你亲眼看到过浩瀚的大海吗
浩瀚的大海中含量最大的是什么物质
除此之外,还蕴藏着哪些资源呢
人们是如何从海水中获得氯化钠和使用氯化钠的
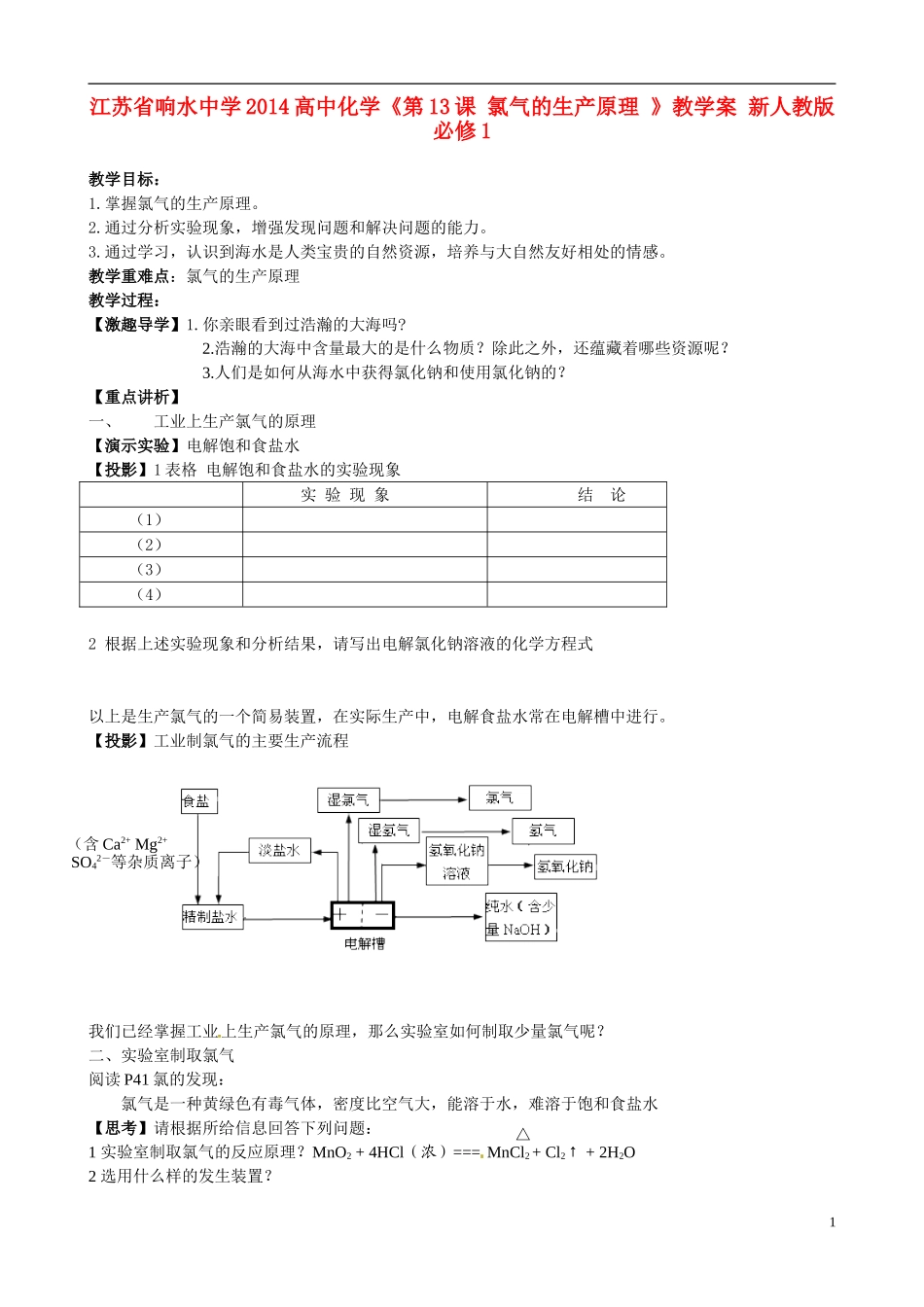
【重点讲析】一、工业上生产氯气的原理【演示实验】电解饱和食盐水【投影】1 表格 电解饱和食盐水的实验现象实 验 现 象结 论(1)(2)(3)(4)2 根据上述实验现象和分析结果,请写出电解氯化钠溶液的化学方程式以上是生产氯气的一个简易装置,在实际生产中,电解食盐水常在电解槽中进行
【投影】工业制氯气的主要生产流程我们已经掌握工业上生产氯气的原理,那么实验室如何制取少量氯气呢
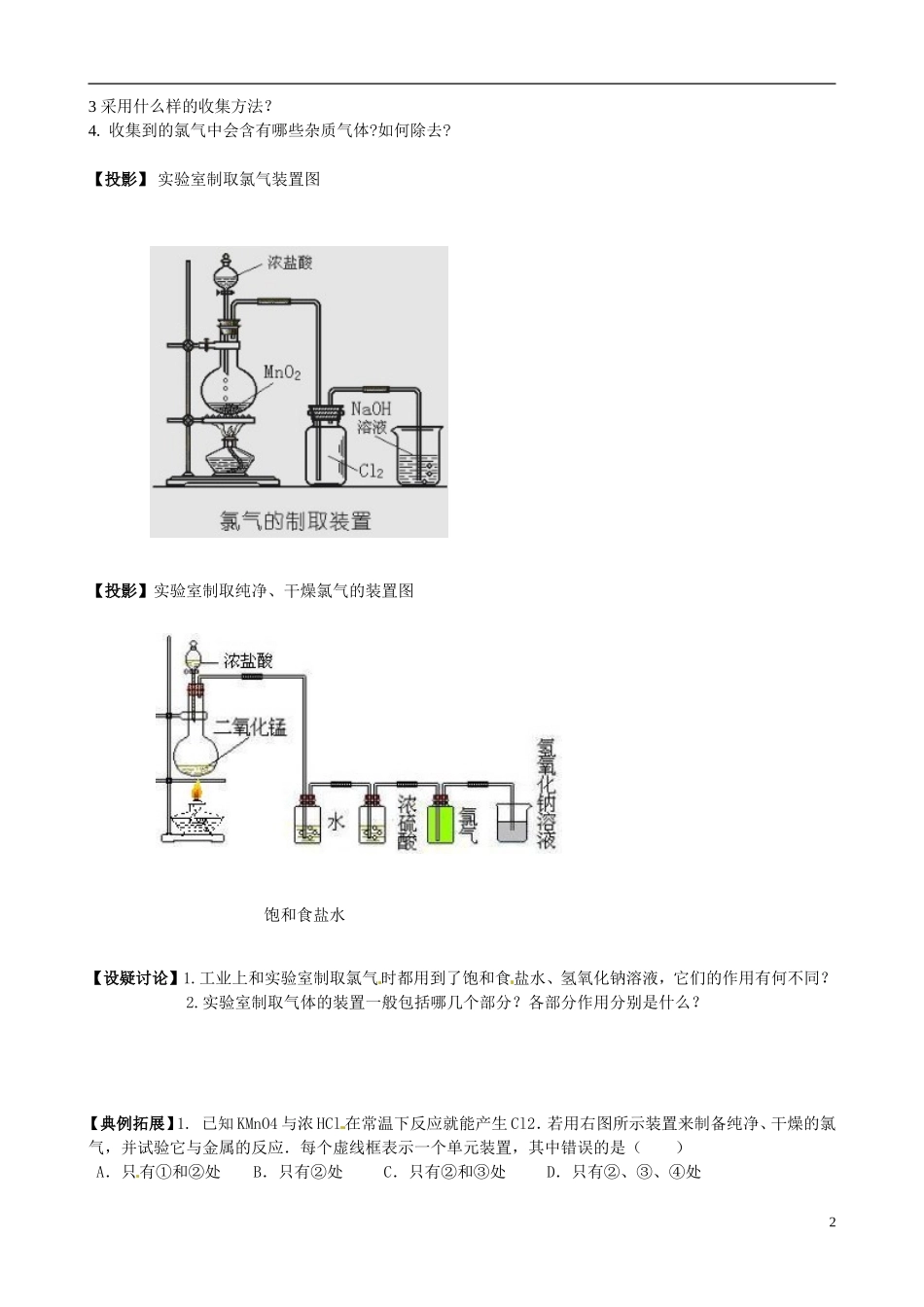
二、实验室制取氯气阅读 P41 氯的发现:氯气是一种黄绿色有毒气体,密度比空气大,能溶于水,难溶于饱和食盐水【思考】请根据所给信息回答下列问题:1 实验室制取氯气的反应原理
MnO2 + 4HCl(浓)=== MnCl2 + Cl2↑ + 2H2O2 选用什么样的发生装置
1△(含 Ca2+ Mg2+ SO42-等杂质离子)3 采用什么样的收集方法
收集到的氯气中会含有哪些杂质气体
【投影】 实验室制取氯气装置图【投影】实验室制取纯净、干燥氯气的装置图【设疑讨论】1
工业上和实验室制取氯气时都用到了饱和食盐水、氢氧化钠溶液,它们的作用有何不同
实验室制取气体的装置一般包括哪几个部分
各部分作用分别是什么
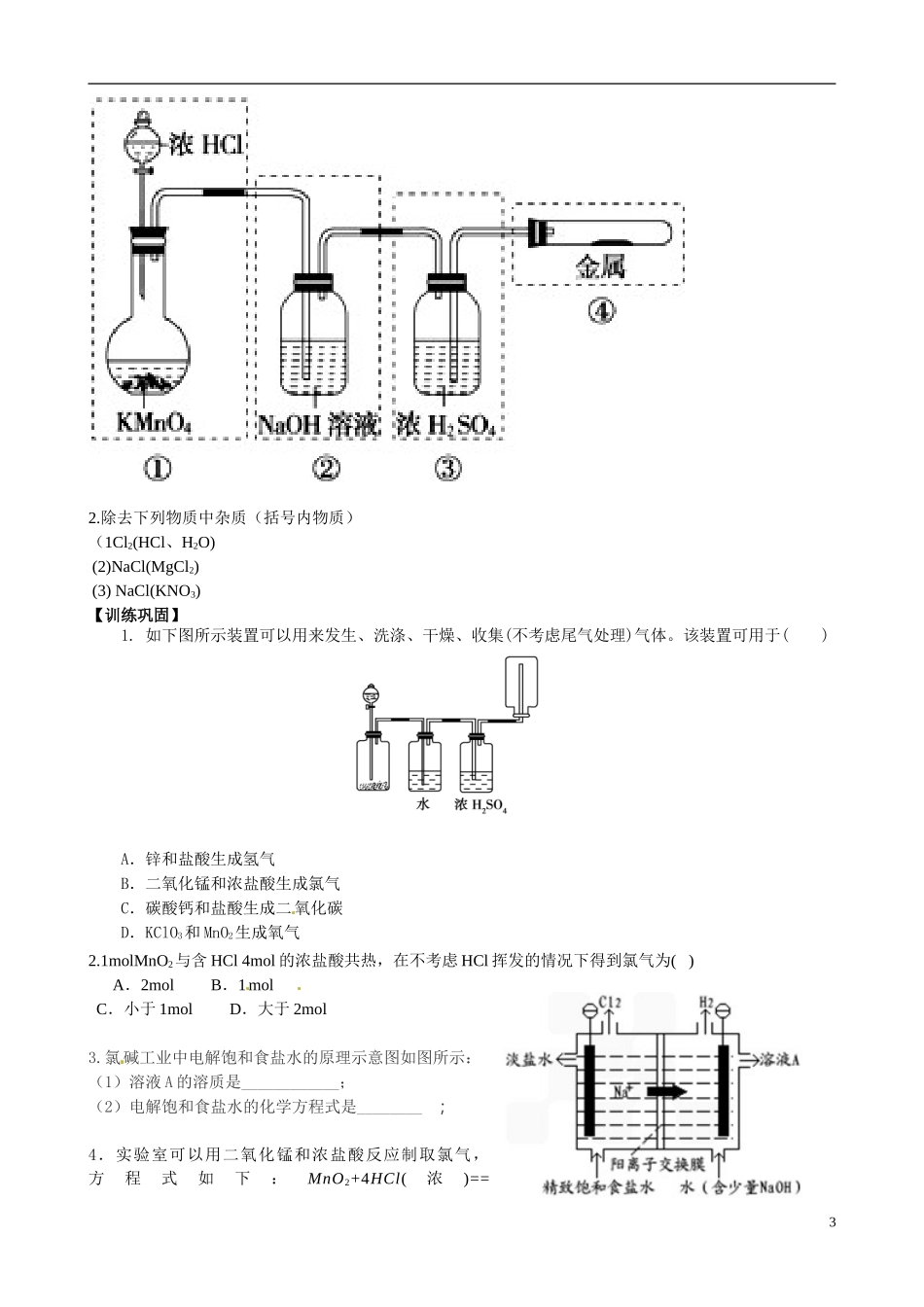
【典例拓展】1
已知 KMnO4 与浓 HCl 在常温下反应就能产生 Cl2.若用右图所示装置来制备纯净、干燥的氯气,并试验它与金属的反