江苏省响水中学 2014 高中化学《第 30 课 含硫化合物的相互转化》教学案 新人教版必修 1【学习目标】1
从硫元素化合价的变化角度理解不同含硫物质之间的相互转化的因素
通过抓住硫元素化合价相同或不同物质间的转化,整理归纳含硫物质的化学性质,培养依据物质的内在联系整理归纳化学知识的能力
通过对含硫物质的分析-综合-再分析-再综合的循环,会逻辑分析与综合的科学方法
【教学重点】含硫物质的相互转化,构建知识网络图
【教学过程】【激趣导学】我们已经学习了 SO2和 H2SO4这两种重要的含硫化合物,你还知道在自然界中哪些物质中存在硫元素吗
在这些物质中硫元素以什么形式存在
火山喷口附近、含硫矿物、石膏(CaSO4·2H2O)、芒硝(Na2SO4·10H2O)等
【重点讲析】 一、硫的性质1、自然界中的硫元素主要以 、 、 等形式存在
2、硫元素的常见化合价有
3、物理性质:颜色 ;俗名 ;溶解性
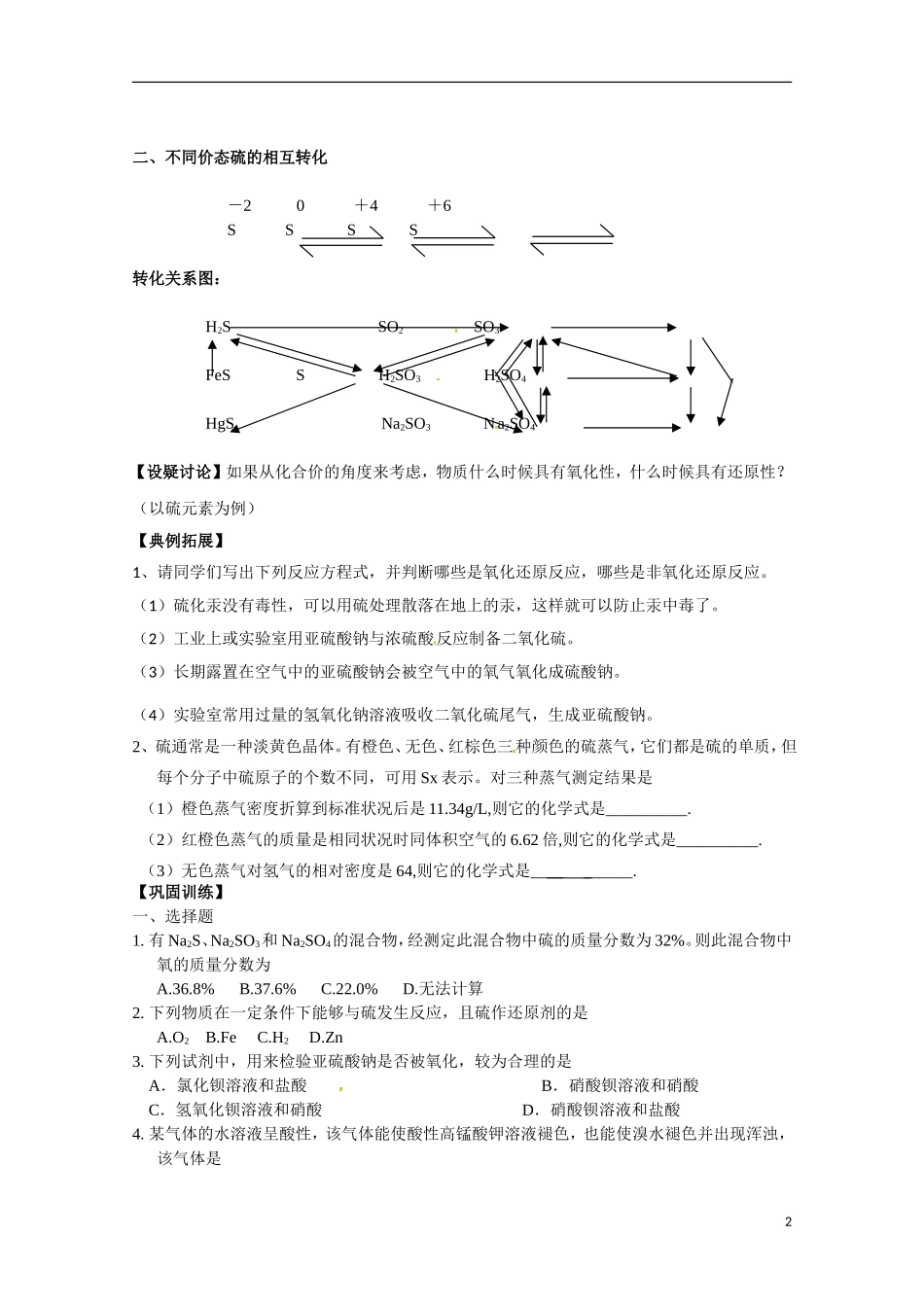
4、化学性质: ① 做氧化剂:H2+S→ Fe+S→ Cu+S→② 做还原剂:S+2H2SO4(浓) △ 3SO2↑+2H2O ③既做氧化剂,又做还原剂 3S+6KOH △ 2K2S+3K2SO3+3H2O(此反应用于除去试管中残留的硫)④ 特性:Hg、Ag 在常温下虽跟 O2不反应,但却易跟 S 反应Hg+S=HgS (此反应用于消除室内洒落的 Hg)5、硫及其化合物性质比较: SSO2H2SO4色态味溶解性 化 学性 质制 取1二、不同价态硫的相互转化 -2 0 +4 +6 S S S S转化关系图:H2S SO2 SO3FeS S H2SO3 H2SO4HgS Na2SO3 Na2SO4【设疑讨论】如果从化合价的角度来考虑,物质什么时候具有氧化性,什么时候具有还原性
(以硫元素为例)【典例拓展】1、请同学们写出下列反应方程式,并判断哪些是氧化还原反应,哪些是非氧化还