辽宁省沈阳铁路实验中学 2014 年高中化学 4
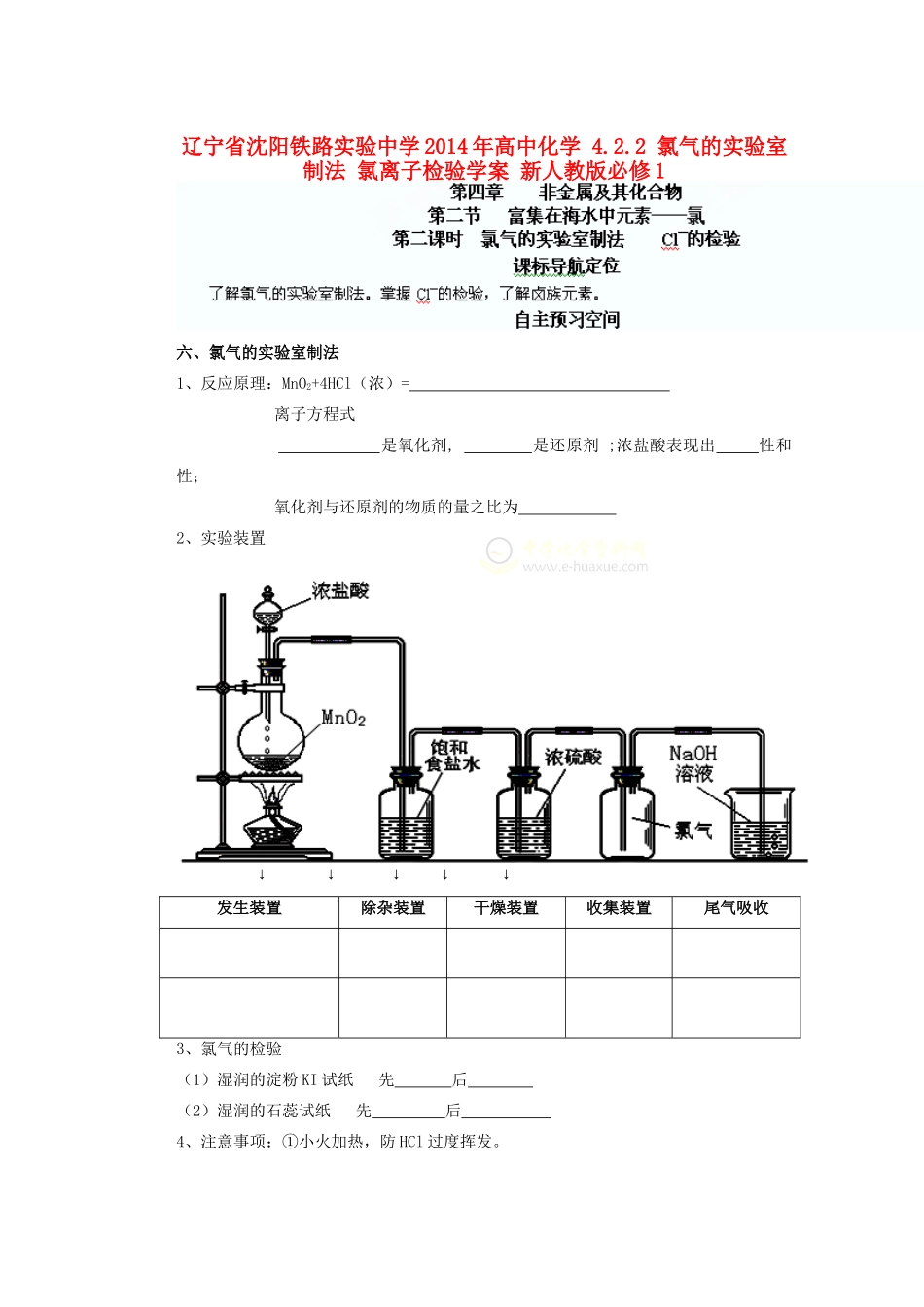
2 氯气的实验室制法 氯离子检验学案 新人教版必修 1六、氯气的实验室制法1、反应原理:MnO2+4HCl(浓)= 离子方程式 是氧化剂, 是还原剂 ;浓盐酸表现出 性和 性; 氧化剂与还原剂的物质的量之比为 2、实验装置 ↓ ↓ ↓ ↓ ↓ 发生装置除杂装置干燥装置收集装置尾气吸收3、氯气的检验(1)湿润的淀粉 KI 试纸 先 后 (2)湿润的石蕊试纸 先 后 4、注意事项:①小火加热,防 HCl 过度挥发
② 收集 Cl2时,导气管应插入集气瓶底部
③ 导气管长进短出
七、氯离子的检验1、检验试剂: 和
2、检验步骤:先在待测溶液中滴加少量的 酸化,再加 溶液
3、反应原理 Ag++Cl-==AgCl↓(离子方程式),AgCl 为 色沉淀,不溶于稀硝酸
4、加稀 HNO3的目的:排除 CO32—等离子的干扰,有关离子反应
八、卤族元素1、在元素周期表中,与氯元素处于同一纵行---第Ⅶ A 族的元素还有 ① 最外层电子都有 个电子,易 个电子;② 都是 ③ 都能与 Na、K、Ca、Mg 等金属化合生成盐,所以统称为卤素(成盐元素之意)
④ 卤素单质都能和活泼金属、氢气、水、碱反应,化学性质相似
2、卤素单质氧化性的比较随元素原子核电荷数的增大,原子半径增大,得电子能力减弱,故氧化性减弱氧化性(非金属性): 离子的还原性 3、卤素单之间相互置换:Cl2 + 2Br- = Cl2 + 2I- = -Br2 + 2I-= 4、卤素单质及其化合物的用途(1)、碘单质(Ⅰ 2)被用于制作碘酊(别名:碘酒)(2)
溴化银(AgBr)被用于制作感光胶卷和变色玻璃(3)
碘化银(AgⅠ)被用于人工降雨【思维拓展】 1、如何检查装置的气密性
2、能否用稀盐酸代替浓盐酸与 MnO2反应制取 Cl2
3、为何用饱和食盐水吸收 Cl2