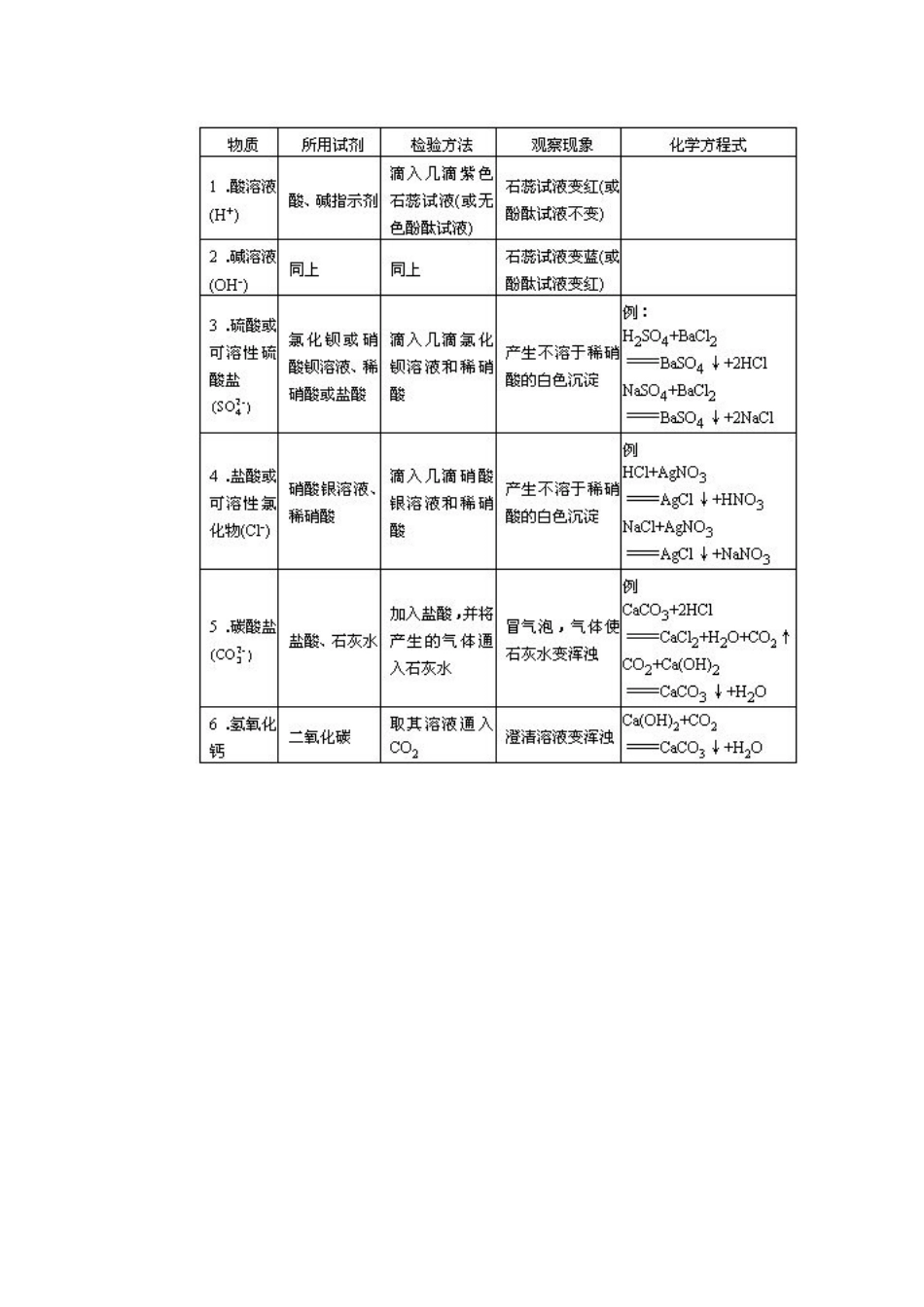
初中化学常见离子的检验一、H+、Ag+、OH-、Cl-、SO42-、CO32- 的检验(1)H+检验
方法 1、将紫色石蕊试液滴入盛有少量待测液的试管中,振荡,假如石蕊试液变红,则证明 H+存在
方法 2、用干燥清洁的玻璃棒蘸取未知液滴在蓝色石蕊试纸上,假如蓝色试纸变红,则证明 H+的存在
方法 3、用干燥清洁的玻璃棒蘸取未知液滴在 pH 试纸上,然后把试纸显示的颜色跟标准比色卡对比,便可知道溶液的 pH,假如 pH 小于 7,则证明 H+的存在
2)Ag+检验
将少量盐酸或少量可溶性的盐酸盐溶液倒入盛有少量待测液的试管中,振荡,假如有白色沉淀生成,再加入少量的稀硝酸,假如沉淀不消逝,则证明 Ag+的存在
(3)OH-的检验
方法 1、将紫色石蕊试液滴入盛有少量待测液的试管中,振荡,假如石蕊试液变蓝,则证明 OH-的存在
方法 2、用干燥清洁的玻璃棒蘸取未知液滴在红色石蕊试纸上,假如红色石蕊试纸变蓝,则证明 OH-的存在
方法 3、将无色的酚酞试液滴入盛有少量待测液的试管中,振荡,假如酚酞试液变红,则证明 OH-的存在
方法 4、干燥清洁的玻璃棒蘸取未知液滴在 pH 试纸上,然后把试纸显示的颜色跟标准比色卡对比,便可知道溶液的 pH,假如 pH 大于 7,则证明 OH-的存在
(4)Cl-的检验
将少量的硝酸银溶液倒入盛有少量待测液的试管中,振荡,假如有白色沉淀生成,再加入少量的稀硝酸,假如沉淀不消逝,则证明 Cl-的存在
(5)SO42-的检验
将少量氯化钡溶液或硝酸钡溶液倒入盛有少量待测液的试管中,振荡,假如有白色沉淀生成,再加入少量的稀硝酸,假如沉淀不消逝,则证明 SO42-的存在
(6)CO32-的检验
将少量的盐酸或硝酸倒入盛有少量待测液的试管中,假如有无色气体放出,将此气体通入盛有少量澄清石灰水的试管中,假如石灰水变浑,则证明原待测液中 CO32-的存在