专题一 增分补课 2 溶解度在高考中的拓展应用[知识查补]1.溶解度在一定温度下,某固体物质在 100_g 溶剂 (通常是水)里达到饱和状态时所溶解的质量,叫做这种物质在该溶剂里的溶解度,其单位为“g”
固体物质溶解度(饱和溶液)S=影响溶解度大小的因素(1)内因:物质本身的性质(由结构决定)
(2)外因:① 溶剂的影响(如 NaCl 易溶于水不易溶于汽油)
② 温度的影响:升温,大多数固体物质的溶解度增大,少数物质却相反,如 Ca(OH)2;温度对 NaCl 的溶解度影响不大
2.溶解度曲线(1)定义:溶解度曲线是同种物质在不同温度下的溶解度绘制出来的曲线,一般随着温度的升高而升高,但是少部分物质会随着温度的升高而降低
由于固体物质的溶解度随温度变化而变化,该变化可以用溶解度曲线来表示;用纵坐标表示溶解度,横坐标表示温度,绘出固体物质的溶解度随温度变化的曲线就叫做溶解度曲线
(2)意义:① 表示同一种物质在不同温度时的溶解度或溶解度随温度变化的情况;② 表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小
若两种物质的溶解度曲线相交,则在该温度下两种物质的溶解度相等;③ 根据溶解度曲线可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法;可以用冷却热饱和溶液或蒸发溶剂;④ 根据溶解度曲线能进行有关的计算
要在一定的温度下,溶液质量、溶剂质量,溶解度这是进行溶解度计算所要的四个重要条件
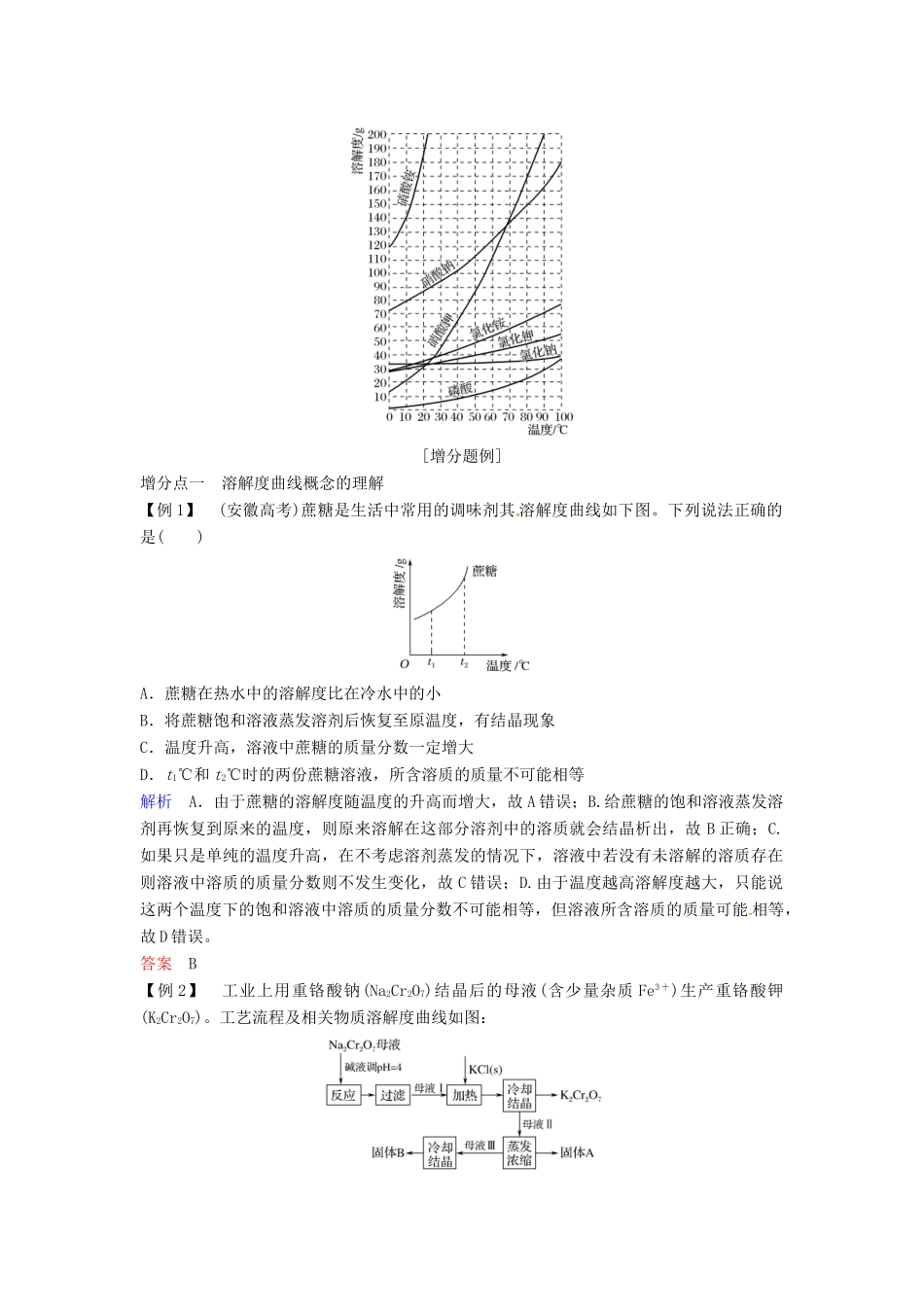
(3)曲线举例[增分题例]增分点一 溶解度曲线概念的理解【例 1】 (安徽高考)蔗糖是生活中常用的调味剂其 溶解度曲线如下图
下列说法正确的是( )A.蔗糖在热水中的溶解度比在冷水中的小B.将蔗糖饱和溶液蒸发溶剂后恢复至原温度,有结晶现象C.温度升高,溶液中蔗糖的质量分数一定增大D.t1℃和 t2℃时的两份蔗糖溶液,所含溶质的质量不可能相等解析 A.由于蔗糖的溶解