[考法综述] 化学平衡移动和化学反应速率在高考中经常联系在一起考查,综合性较强,题目较抽象,常以图象或表格形式以选择判断形式出现
除要求掌握一些基本规律外,还要对它们的关系进行归纳和总结
命题法 1 化学平衡移动与化学反应速率的关系典例 1 对处于化学平衡的体系,化学平衡与化学反应速率的因果关系正确的是 ( )选项因果A化学反应速率变化化学平衡一定发生移动B化学平衡不移动化学反应速率一定是在催化剂存在下发生变化C正反应进行的程度大正反应速率一定大D化学平衡发生移动化学反应速率一定发生不同程度的变化 [ 解析 ] A 项,若 v 正、 v 逆同等程度地变化 ( 如使用催化剂 ) ,则平衡不移动,错误 ; B 项,对于反应前后气体分子数不变的反应,增大压强, v 正、 v 逆均增大,但 v 正= v 逆,平衡不发生移动,错误; C 项,反应进行的程度与反应速率的大小无必然联系,错误
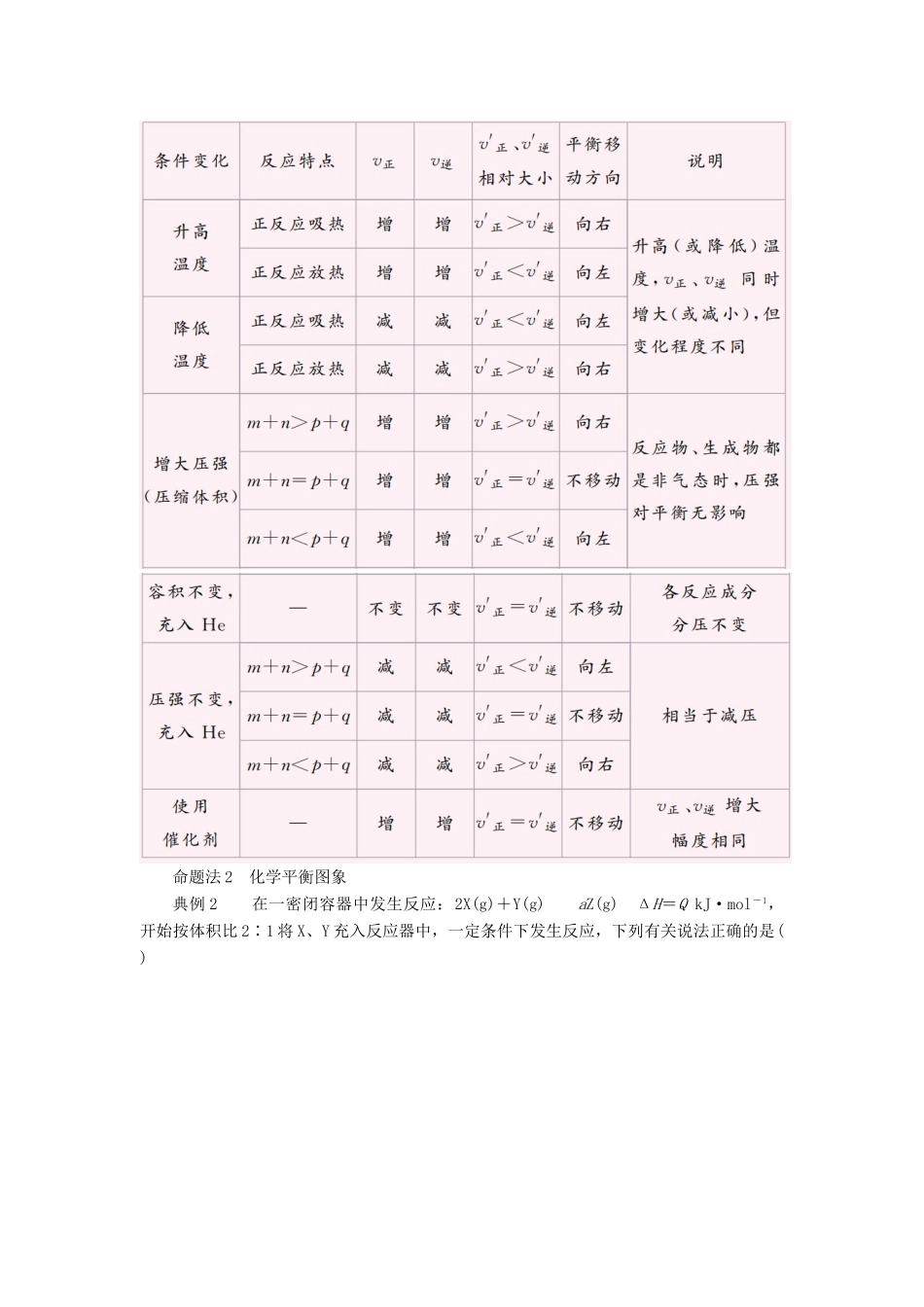
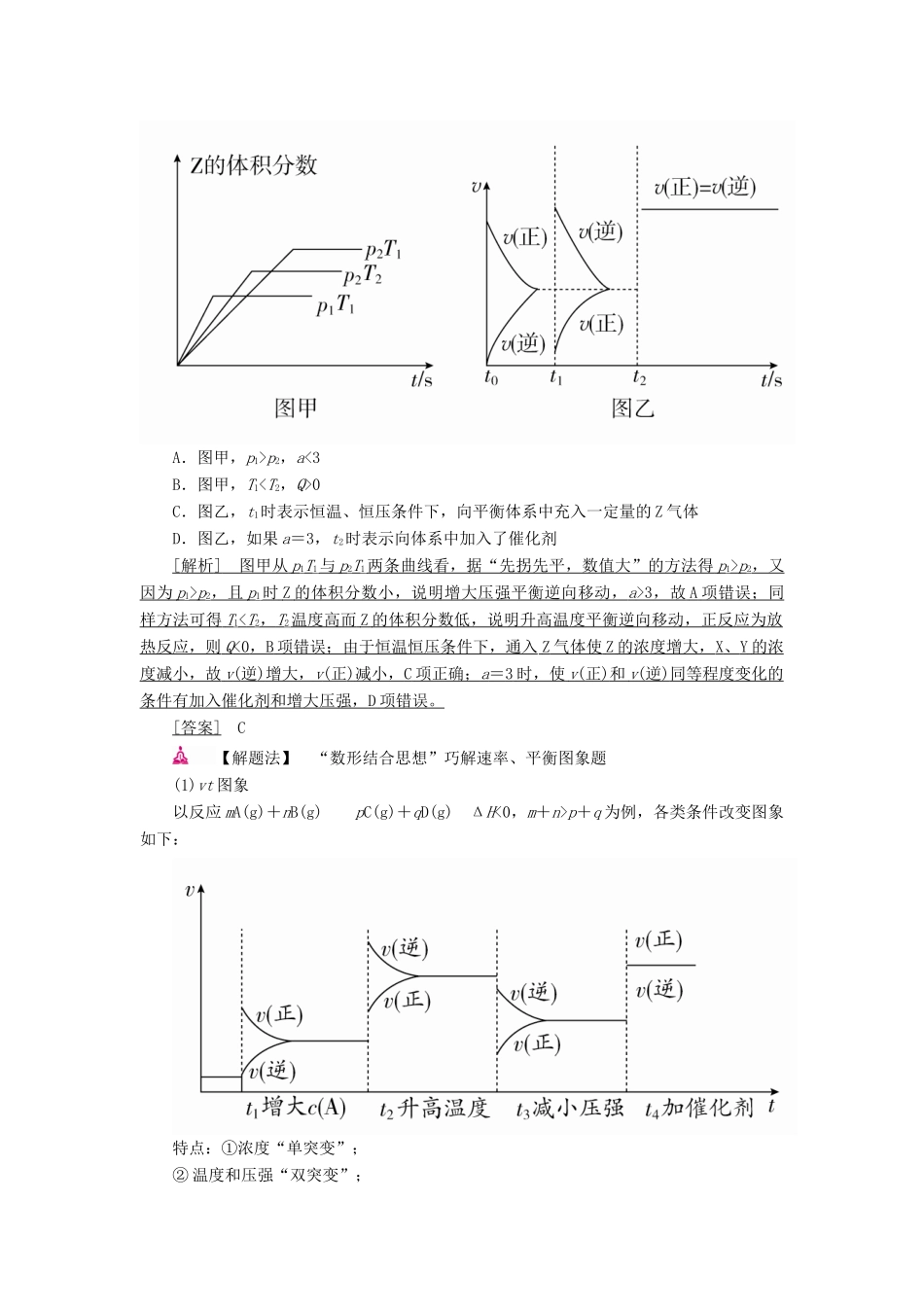
[ 答案 ] D【解题法】 外界条件的变化对速率的影响和平衡移动方向的判断对于反应 mA(g)+nB(g)pC(g)+qD(g)分析如下:命题法 2 化学平衡图象典例 2 在一密闭容器中发生反应:2X(g)+Y(g)aZ(g) ΔH=Q kJ·mol-1,开始按体积比 2∶1 将 X、Y 充入反应器中,一定条件下发生反应,下列有关说法正确的是( )A.图甲,p1>p2,a p 2,又因为 p 1> p 2,且 p 1 时 Z 的体积分数小,说明增大压强平衡逆向移动, a >3 ,故 A 项错误;同 样方法可得 T 1< T 2, T 2 温度高而 Z 的体积分数低,说明升高温度平衡逆向移动,正反应为放 热反应,则 Q