1 电解使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程
2 电解池(或电解槽)(1)定义借助于电流引起氧化还原反应的装置,也就是把电能转化为化学能的装置
(2)构成条件① 有与电源相连的两个电极
② 两个电极插入电解质溶液(或熔融电解质)中
③ 形成闭合回路
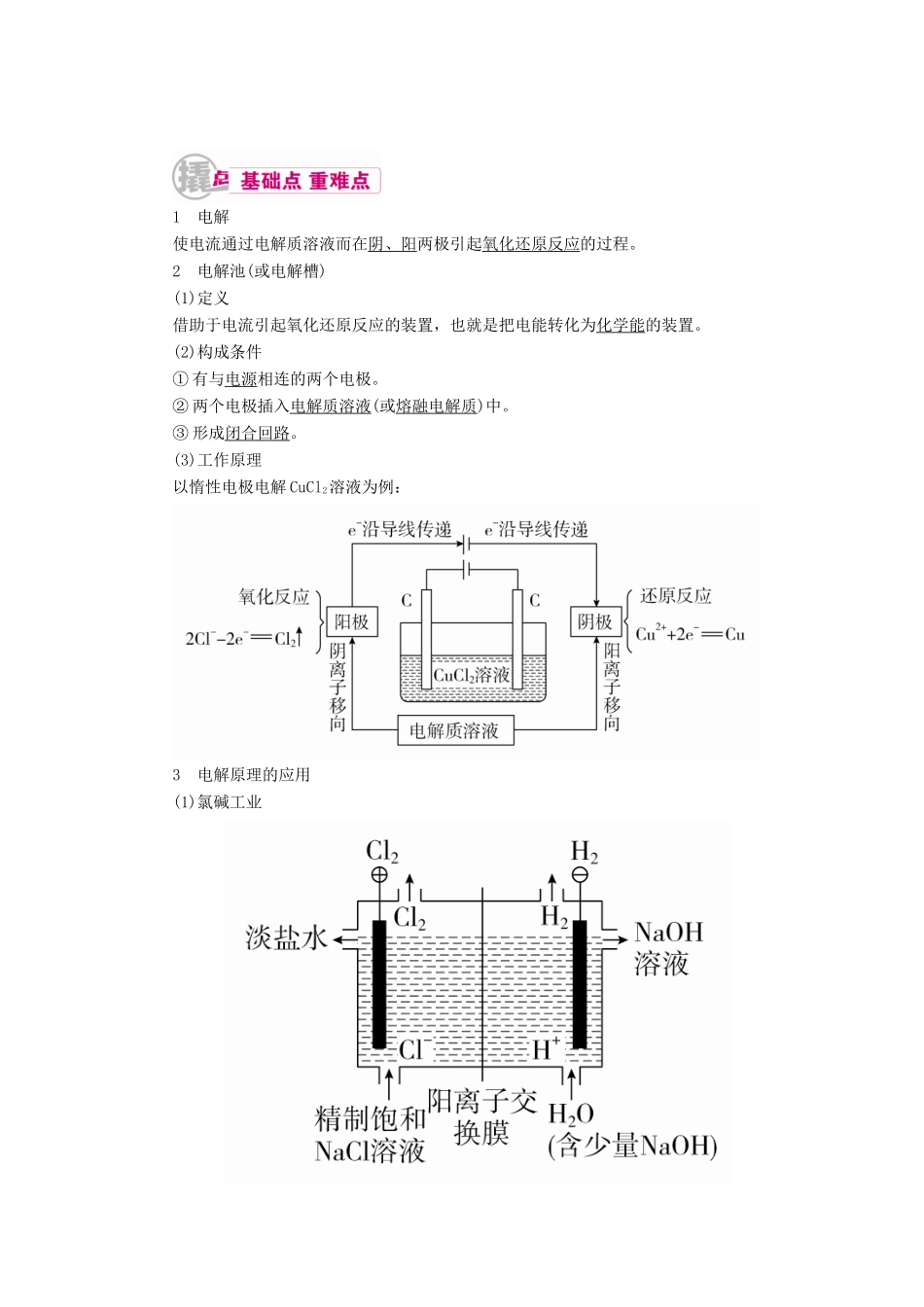
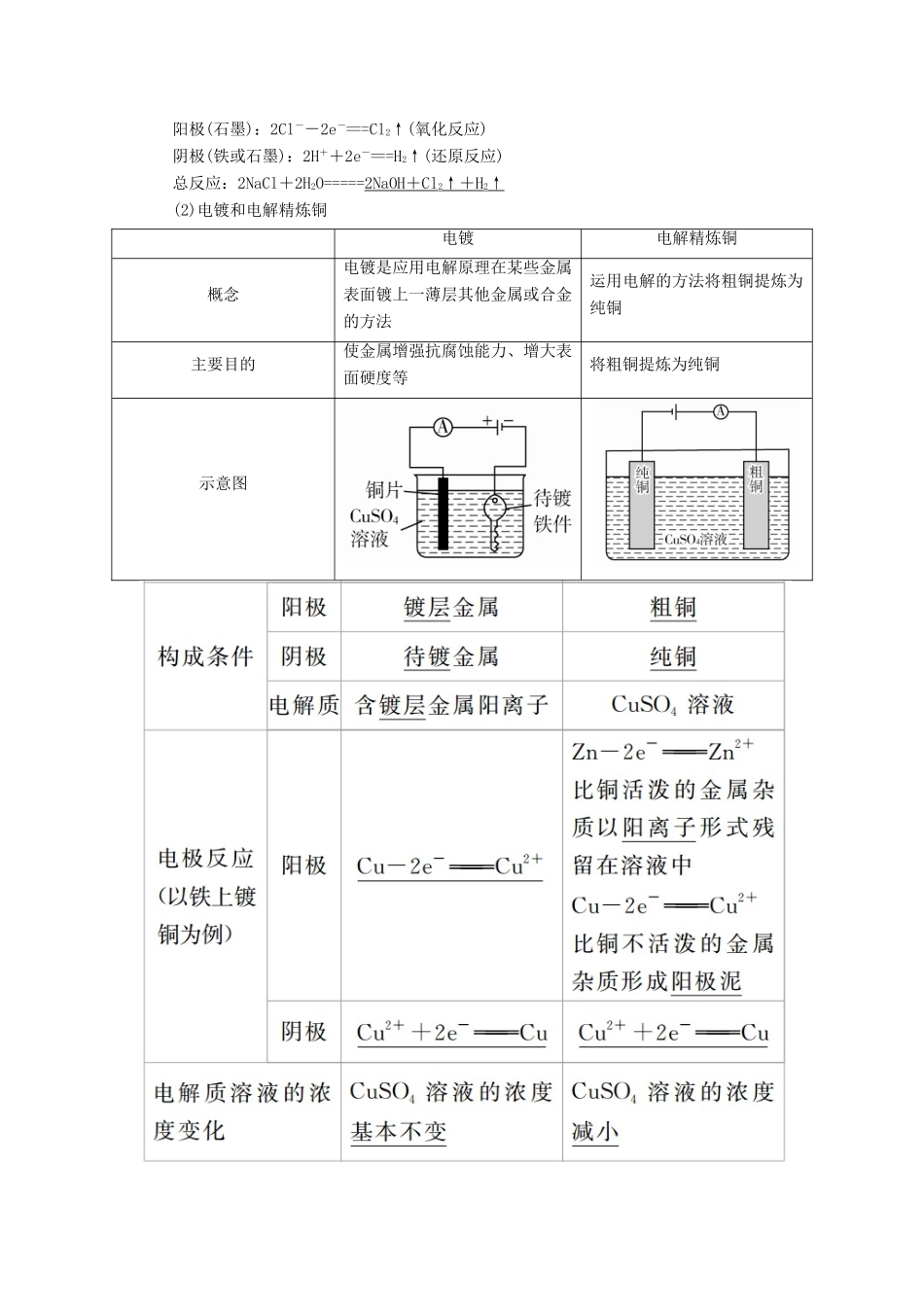
(3)工作原理以惰性电极电解 CuCl2溶液为例:3 电解原理的应用(1)氯碱工业阳极(石墨):2Cl--2e-===Cl2↑(氧化反应)阴极(铁或石墨):2H++2e-===H2↑(还原反应)总反应:2NaCl+2H2O=====2NaOH + Cl 2↑ + H 2↑(2)电镀和电解精炼铜电镀电解精炼铜概念电镀是应用电解原理在某些金属表面镀上一薄层其他金属或合金的方法运用电解的方法将粗铜提炼为纯铜主要目的使金属增强抗腐蚀能力、增大表面硬度等将粗铜提炼为纯铜示意图(3)冶炼金属① 电解熔融 NaCl 制取金属钠NaCl 在高温下熔融,并发生电离:NaCl===Na++Cl-;通直流电后,阴极:2Na ++2e -===2Na,阳极:2Cl --2e -===Cl2↑,总反应:2NaCl(熔融)=====2Na+Cl2↑② 电解熔融 MgCl2制取金属镁阴极:Mg2++2e-===Mg阳极:2Cl--2e-===Cl2↑总反应:MgCl2(熔融)=====Mg+Cl2↑③ 电解熔融 Al2O3制取金属铝阴极:4Al3++12e-===4Al阳极:6O2--12e-===3O2↑总反应:2Al2O3(熔融)=====4Al+3O2↑学霸巧学卡 电解原理应用时注意事项(1)阳离子交换膜(以电解 NaCl 溶液为例),只允许阳离子(Na+)通过,而阻止阴离子(Cl-、OH-)和分子(Cl2)通过,这样既能防止 H2和 Cl2混合爆炸,又能避免 Cl2和 NaOH 溶液作用生成 NaClO 影响烧碱质量
(2)电解或