专题十二 电化学考纲展示 命题探究1 原电池(1)概念把化学能转化为电能的装置
(2)反应本质发生氧化还原反应
(3)构成条件① 一看反应看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)
② 二看两电极:一般是活泼性不同的两电极
③ 三看是否形成闭合回路
形成闭合回路需三个条件:a.电解质溶液;b.两电极直接或间接接触;c.两电极插入电解质溶液
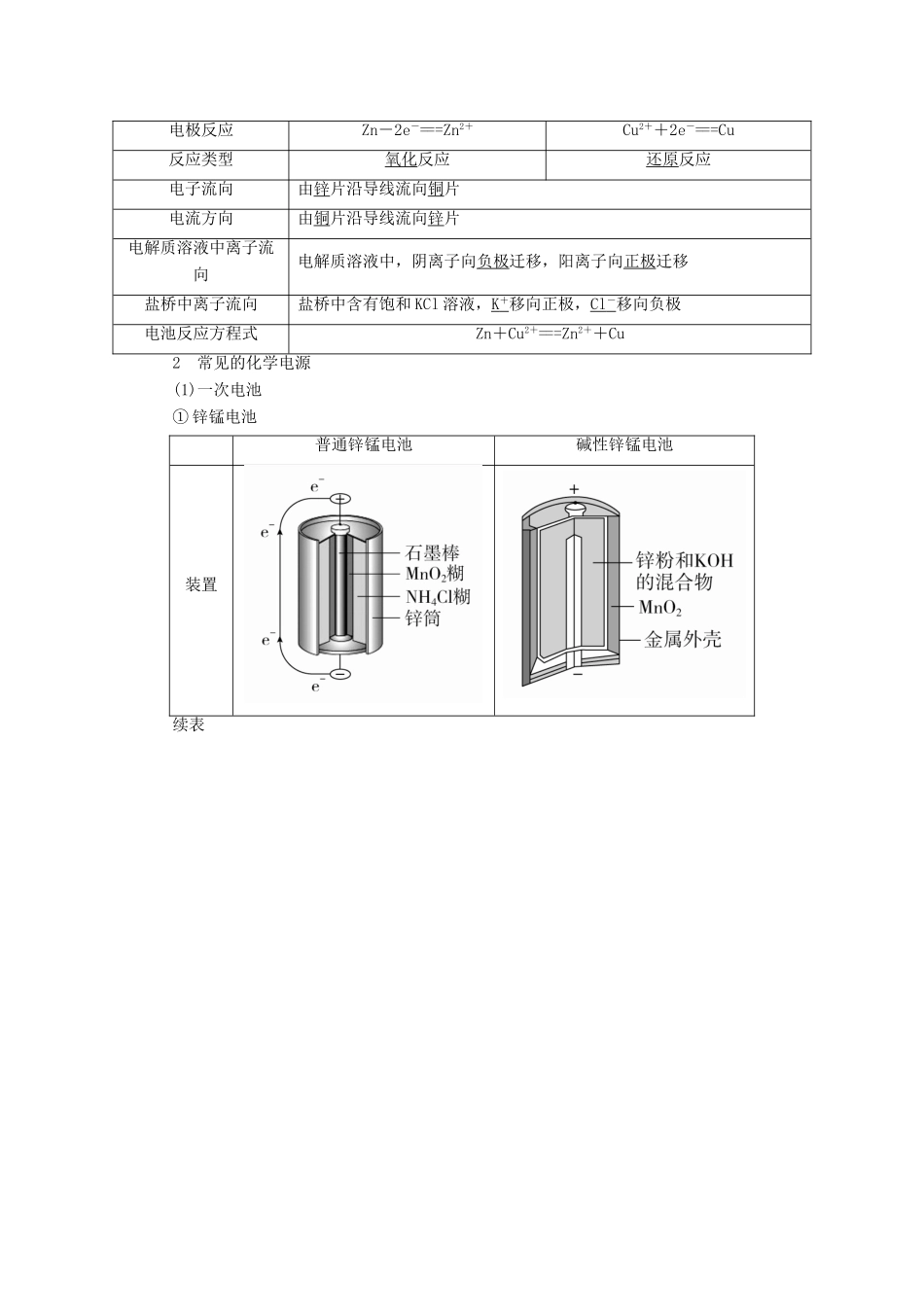
(4)工作原理(以铜-锌原电池为例)装置图 单液原电池 双液原电池续表电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电子流向由锌片沿导线流向铜片电流方向由铜片沿导线流向锌片电解质溶液中离子流向电解质溶液中,阴离子向负极迁移,阳离子向正极迁移盐桥中离子流向盐桥中含有饱和 KCl 溶液,K + 移向正极,Cl - 移向负极电池反应方程式Zn+Cu2+===Zn2++Cu2 常见的化学电源(1)一次电池① 锌锰电池普通锌锰电池碱性锌锰电池装置续表② 银锌纽扣电池(电解质溶液为 KOH 溶液)负极材料:Zn电极反应:Zn-2e-+2OH-===Zn(OH)2正极材料:Ag2O电极反应:Ag2O+2e-+H2O===2Ag+2OH-总反应:Zn+Ag2O+H2O===2Ag+Zn(OH)2(2)二次电池(可充电电池)① 铅蓄电池(电解质溶液为 30%H2SO4溶液)a.放电时的反应负极:Pb(s)+SO(aq)-2e-===PbSO4(s) (氧化反应)正极:PbO2(s)+4H+(aq)+SO(aq)+2e-===PbSO4(s) + 2H 2O(l) (还原反应)总反应:Pb(s)+PbO2(s)+2H2SO4(aq)===2PbSO4(s) + 2H 2O(l)b.充电时的反应阴极:PbSO4(s)+2e-===Pb(s) + SO(aq)