专题十三 钠及其化合物考纲展示 命题探究1 钠(1)物理性质颜色熔点硬度密度导电导热性银白色低小比水的小比煤油的大良好(2)化学性质① 与非金属单质反应O2Cl2:2Na+Cl2===2NaCl(黄色火焰、白烟)S:2Na+S===Na2S(研磨爆炸)② 与 H2O 反应2Na+2H2O===2NaOH + H 2↑现象:③ 与酸溶液反应(如 HCl)2Na+2HCl===2NaCl + H 2↑④ 与盐反应a.与熔融盐反应如:4Na+TiCl4=====4NaCl+TiNa+KCl=====NaCl+K↑(制取金属钾,因为钾的沸点比钠的低,使钾成为蒸气而逸出)b.与盐溶液反应如:2Na+2NH4Cl===2NaCl + H 2↑ + 2NH 3↑2Na+CuSO4+2H2O===Na2SO4+ H 2↑ + Cu(OH) 2↓⑤ 与某些有机物反应如:2Na+2CH3CH2OH―→2CH3CH2ONa+H2↑2Na+2CH3COOH―→2CH3COONa+H2↑ (3)钠的制备与保存① 钠在自然界以化合态形式存在
工业上通常用电解熔融氯化钠的方法制备钠:2NaCl(熔融)=====2Na+Cl2↑
② 金属钠保存在煤油或石蜡中,使之隔绝空气与水
(4)钠的用途① 制取 Na2O2等化合物
② 钠、钾合金 ( 液态 ) 可用于原子反应堆的导热剂
③ 用作电光源,制作高压钠灯
④ 冶炼某些金属
金属钠具有强的还原性,熔融状态下可以用于制取金属,如 4Na+TiCl4=====4NaCl+Ti
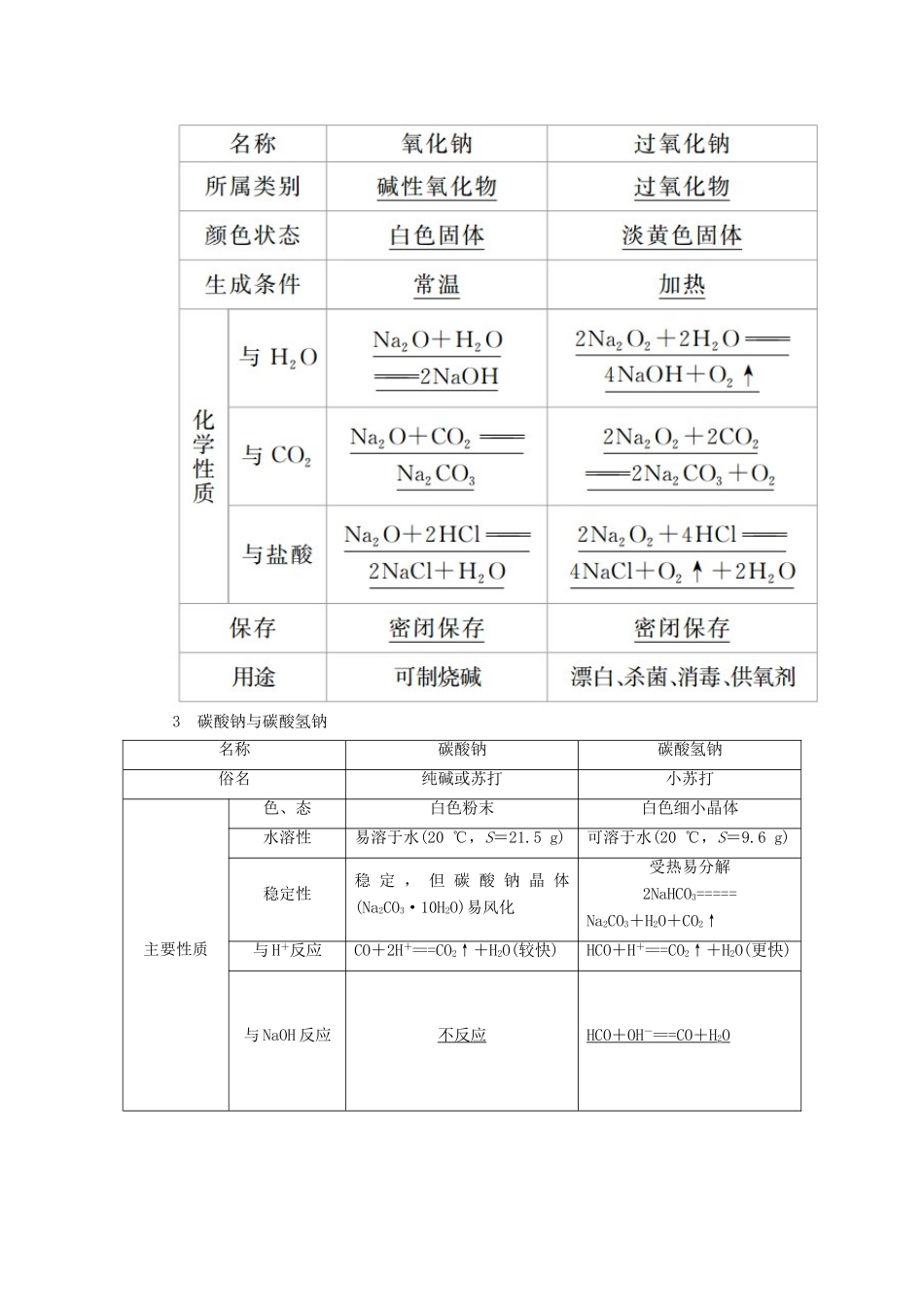
2 氧化钠和过氧化钠名称氧化钠过氧化钠化学式Na2ONa2O2氧元素化合价- 2 - 1 电子式阴阳离子个数比1∶21∶2化学键离子键离子键和共价键(非极性共价键)化合物类型离子化合物离子化合物续表3 碳酸钠与碳酸氢钠名称碳酸钠碳酸氢钠俗名纯碱或苏打小苏打主要性质色、态白色粉末白色细小晶体