专题五 化学能与热能专题五 化学能与热能考纲展示 命题探究1 焓变、反应热(1)焓(H):用于描述物质所具有能量的物理量
(2)焓变(ΔH):ΔH=H ( 生成物 ) - H ( 反应物 )
单位 kJ/mol 或 kJ·mol - 1
(3)反应热:指当化学反应在一定温度下进行时,反应所放出或吸收的热量,通常用符号 Q 表示,单位 kJ/mol 或 kJ·mol - 1
(4)焓变与反应热的关系:对于等压条件下进行的化学反应,如果反应中物质的能量变化全部转化为热能,则有如下关系:Δ H = Q p
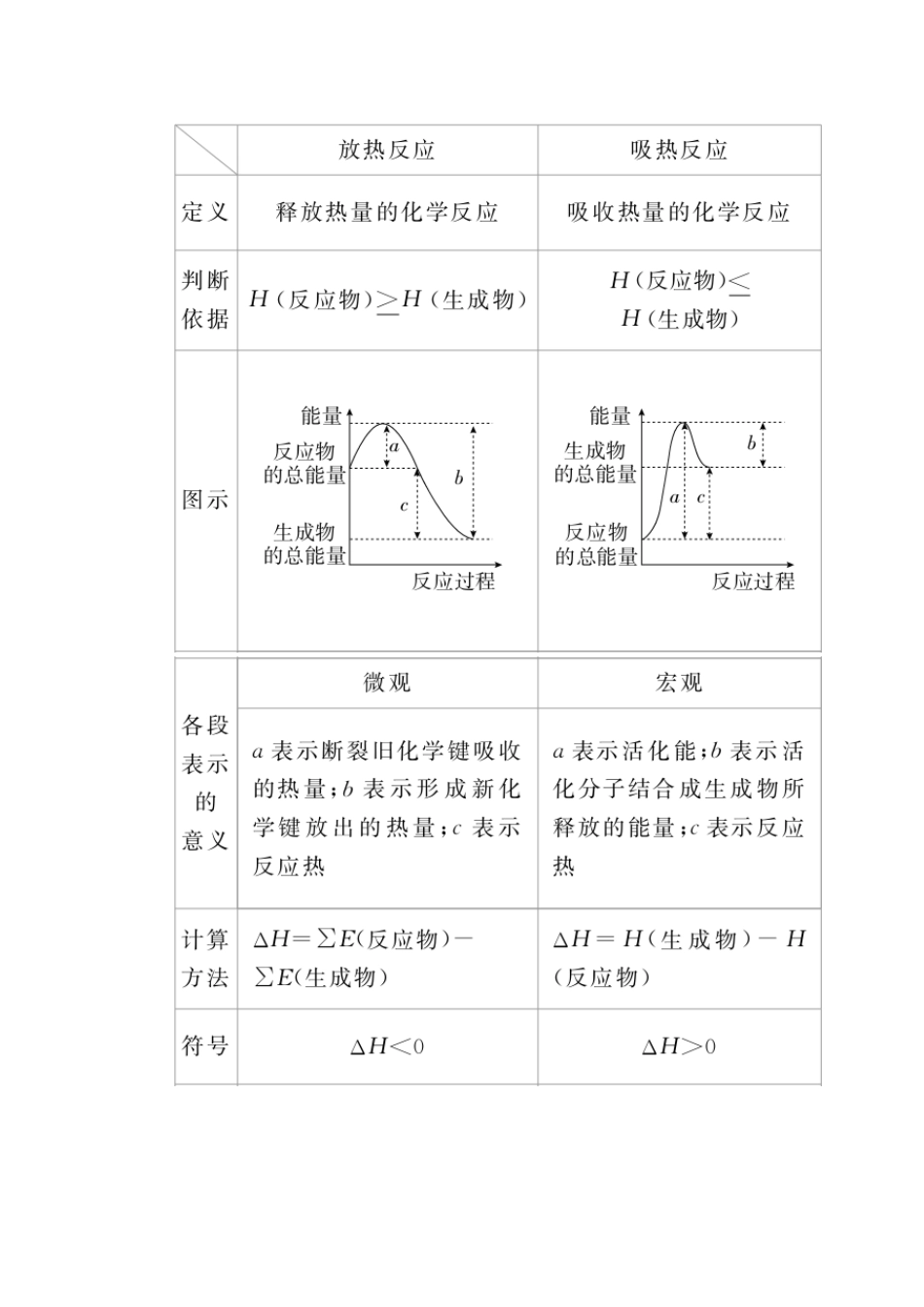
(5)规定:放热反应的 ΔH 为“-”,吸热反应的 ΔH 为“+”
2 燃烧热(1)概念:在 25 ℃、101 kPa 时,1_mol 纯物质 完全燃烧生成稳定的氧化物时所放出的热量
(2)条件:在 25 ℃、101 kPa 下测定
规定可燃物的物质的量为 1_mol
因此,表示可燃物的燃烧热的热化学方程式中,可燃物的化学计量数为 1,其他物质的化学计量数常出现分数
3 中和热(1)概念:在稀溶液中,酸和碱发生中和反应生成 1_mol_H2O(l)时的反应热
(2)中和热的表示:H+(aq)+OH-(aq)===H2O(l) ΔH=-57
3 kJ·mol-1
(3)条件:中和反应的对象为稀溶液;以生成 1_mol H2O(l)为基准,因此表示中和热的热化学方程式中,水的化学计量数为 1,酸、碱或盐的化学计量数可以为分数
(4)中和热的测定实验① 装置如图(在横线上填出仪器的名称)② 注意事项a.碎泡沫塑料及泡沫塑料板的作用是保温隔热,防止热量散失
b.为保证酸、碱完全中和,常使酸或碱稍稍过量
c.实验中若使用弱酸或弱碱,会使测得数值偏小
③ 测定原理ΔH=-(其中:c=4
18 J·g-1· ℃-1=4
18×10-3 kJ·g-1· ℃-1;n 为生成 H2O 的物质