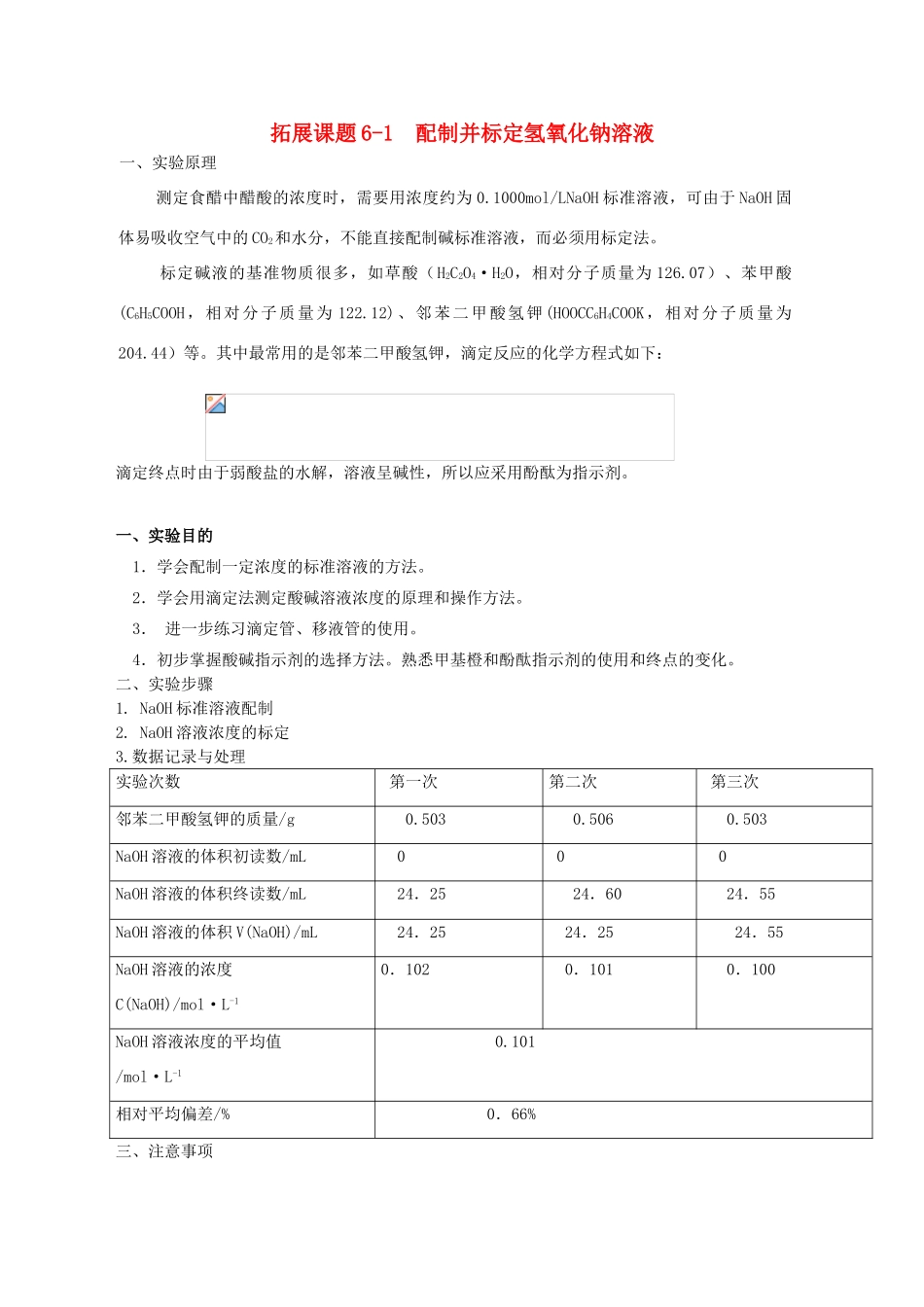
拓展课题 6-1 配制并标定氢氧化钠溶液一、实验原理 测定食醋中醋酸的浓度时,需要用浓度约为 0.1000mol/LNaOH 标准溶液,可由于 NaOH 固体易吸收空气中的 CO2和水分,不能直接配制碱标准溶液,而必须用标定法。 标定碱液的基准物质很多,如草酸(H2C2O4·H2O,相对分子质量为 126.07)、苯甲酸(C6H5COOH,相对分子质量为 122.12)、邻苯二甲酸氢钾(HOOCC6H4COOK,相对分子质量为204.44)等。其中最常用的是邻苯二甲酸氢钾,滴定反应的化学方程式如下:滴定终点时由于弱酸盐的水解,溶液呈碱性,所以应采用酚酞为指示剂。一、实验目的1.学会配制一定浓度的标准溶液的方法。2.学会用滴定法测定酸碱溶液浓度的原理和操作方法。3. 进一步练习滴定管、移液管的使用。4.初步掌握酸碱指示剂的选择方法。熟悉甲基橙和酚酞指示剂的使用和终点的变化。二、实验步骤 1. NaOH 标准溶液配制2. NaOH 溶液浓度的标定3.数据记录与处理实验次数 第一次第二次 第三次邻苯二甲酸氢钾的质量/g 0.503 0.506 0.503NaOH 溶液的体积初读数/mL0 0 0NaOH 溶液的体积终读数/mL24.25 24.60 24.55NaOH 溶液的体积 V(NaOH)/mL24.2524.2524.55NaOH 溶液的浓度C(NaOH)/mol·L-10.102 0.101 0.100NaOH 溶液浓度的平均值/mol·L-1 0.101 相对平均偏差/% 0.66%三、注意事项(1)称量邻苯二甲酸氢钾时,所用锥形瓶外壁要干燥并编号(以后称量同)。(2)NaOH 饱和溶液侵蚀性很强,长期保存最好用聚乙烯塑料化学试剂瓶贮存(用一般的饮料瓶会因被腐蚀而瓶底脱落)。在一般情况下,可用玻璃瓶贮存,但必须用橡皮塞。(3)NaOH 标准溶液配制时,一定量蒸馏水中所加 NaOH 饱和溶液的量随室温的不同而变化,因氢氧化钠在不同温度下的溶解度有差异。夏天(30℃)大约是 5.6mL 饱和氢氧化钠溶液加新煮沸而迅速冷却的蒸馏水到 1000mL;春秋天(2 1℃)大约是 6.2mL 饱和氢氧化钠溶液加新煮沸而迅速冷却的蒸馏水到1000mL;冬天(10℃)大约是 6.7mL 饱和氢氧化钠溶液加新煮沸而迅速冷却的蒸馏水到1000 mL。