化学选修 3《第二章 分子结构与性质》知识点总结一.共价键1.共价键的本质及特征共价键的本质是在原子之间形成共用电子对,其特征是具有饱和性和方向性
2.共价键的类型 ① 按成键原子间共用电子对的数目分为单键、双键、三键
② 按共用电子对是否偏移分为极性键、非极性键
③ 按原子轨道的重叠方式分为 σ 键和 π 键,前者的电子云具有轴对称性,后者电子云具有镜像对称性
3.键 参数 ① 键能:气态基态原子形成 1 mol 化学键释放的最低能量,键能越大,化学键越稳定
② 键长:形成共价键的两个原子之间的核间距,键长越短,共价键越稳定
③ 键角:在原子数超过 2 的分子中,两个共价键之间的夹角
④ 键参数对分子性质的影响键长越短,键能越大,分子越稳定.4.等电子原理原子总数相同、价电子总数相同的分子具有相似的化学键特征,它们的许多性质相近
如CO 和 N2、CO2和 N2O
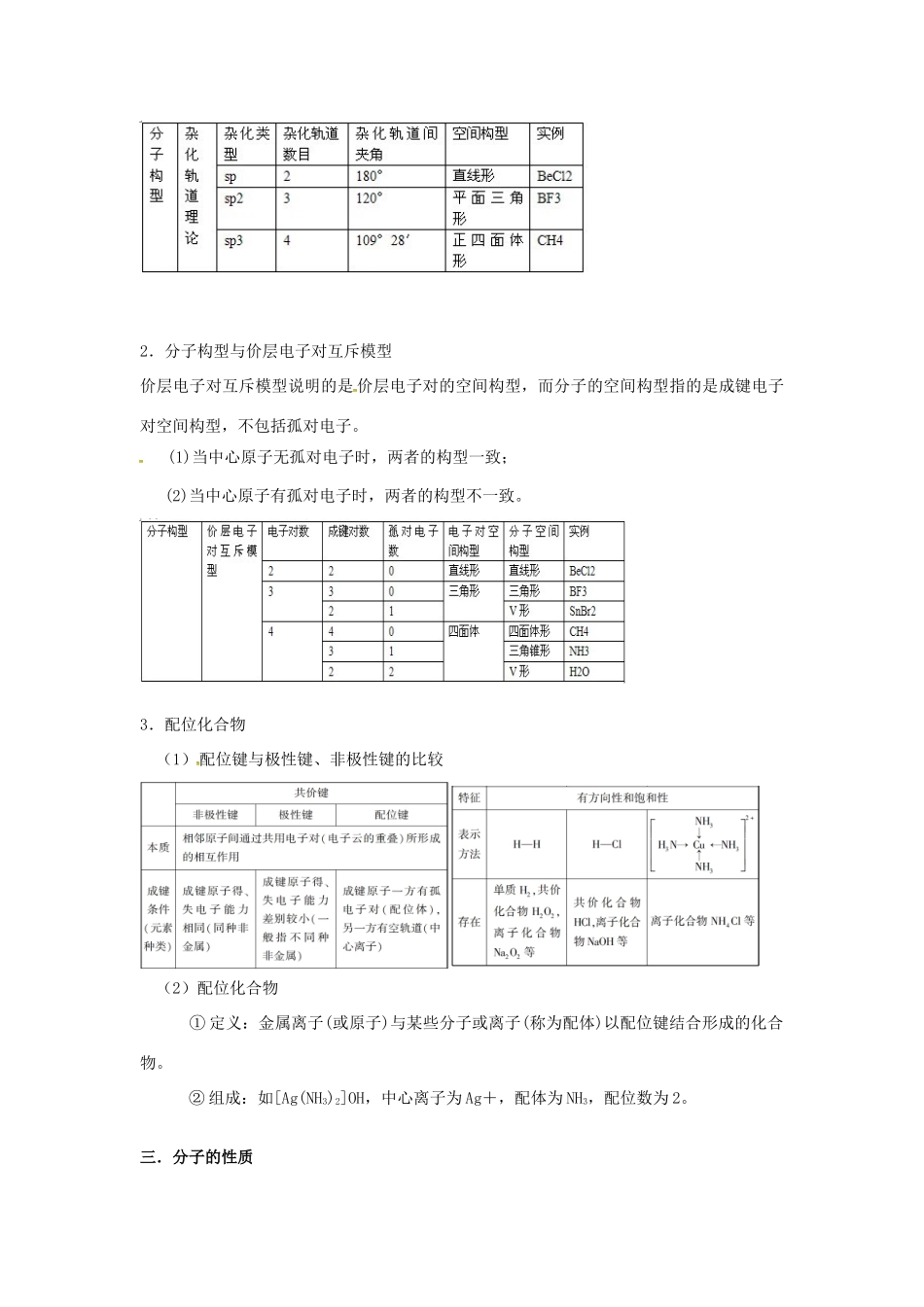
二.分子的立体构型1.分子构型与杂化轨道理论杂化轨道的要点当原子成键时,原子的价电子轨道相互混杂,形成与原轨道数相等且能量相同的杂化轨道杂化轨 道数不同,轨道间的夹角不同,形成分子的空间形状不同
2.分子构型与价层电子对互斥模型价层电子对互斥模型说明的是 价层电子对的空间构型,而分子的空间构型指的是成键电子对空间构型,不包括孤对电子
(1)当中心原子无孤对电子时,两者的构型一致; (2)当中心原子有孤对电子时,两者的构型不一致
3.配位化合物 (1)配位键与极性键、非极性键的比较 (2)配位化合物 ① 定义:金属离子(或原子)与某些分子或离子(称为配体)以配位键结合形成的化合物
② 组成:如[Ag(NH3)2]OH,中心离子为 Ag+,配体为 NH3,配位数为 2
三.分子的性质1.分子间作用力的比较2.分子的极性 (1)极性分子:正电中心和负电中心不重合的分子
(2)非极性分子:正电中心和负电中