第一节 空气的成分第四单元 我们周围的空气1
通过测定空气中氧气含量的实验认识空气的组成,学习从混合气体中除去某种气体进而测定其含量的方法
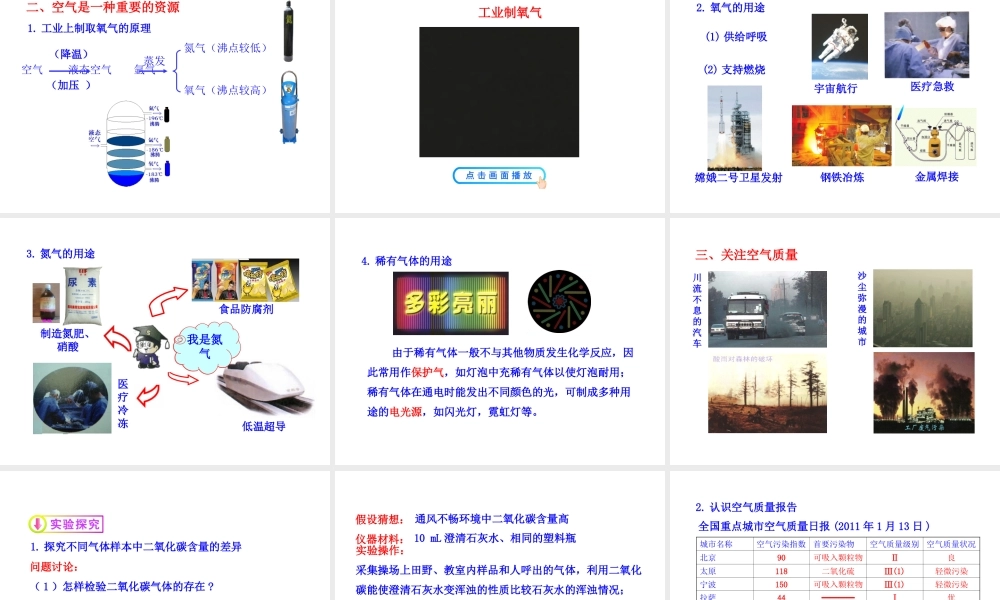
了解空气是一种重要的资源
了解空气污染的危害,认识空气质量报告,增强环保意识和责任感
一、认识空气的组成氩气 ( 0
934%)其他气体 ( 0
02 %)二氧化碳 ( 0
033 %)1
空气成分(体积分数)氮气( 78 %)氧气( 21 %)其他气体提出问题:空气中约含 1/5 体积的氧气,你能通过实验测定空气中氧气的含量吗
思路 1 :将其他气体除去,只剩下氧气,测定氧气体积
思路 2 :将氧气除去,然后通过减少的体积来测定氧气的体积
测定空气中氧气的含量 实验装置 在加热的条件下,铜粉跟空气中的氧气完全反应,生成固体氧化铜,而又不产生新的气体,从而使密闭装置内空气的体积减少,减少的体积即为空气中氧气的体积
实验原理 ( 1 )将一只具支试管注满水,塞上橡胶塞
然后打开橡胶塞,将水倒入量筒中,记录体积
( 2 )如图所示:在另一只具支试管中装入铜粉,塞上橡胶塞,用小气球封闭试管的支管口
移动注射器活塞在注射器内留有一定体积的气体,记录体积后插入橡胶塞
据酒精灯的高度安装仪器
( 3 )用酒精灯在铜粉部位加热,加热时不断推拉注射器
( 4 )停止加热后,待试管冷却至室温,将气球内的气体全部挤入注射器内
待注射器活塞稳定后,记录注射器中气体的体积
实验步骤 具支试管内气体的体积 V1注射器内的气体体积 V2反应结束后注射器中气体体积 V3氧气占空气的体积分数=(V2-V3)/(V1+V2) ×100 % 与真实结果的比较(偏大或偏小)请同学们按要求进行实验,并在下表中记录数据:实验结论: 氧气约占空气体积的 1/5
注意事项④ 冷却到室温读数
① 装置不漏气;② 铜粉足量且反应时间足够;③ 用酒精