专题五分子、晶体结构与性质非选择题1
(2013山东理综,32,8分)卤族元素包括F、Cl、Br等
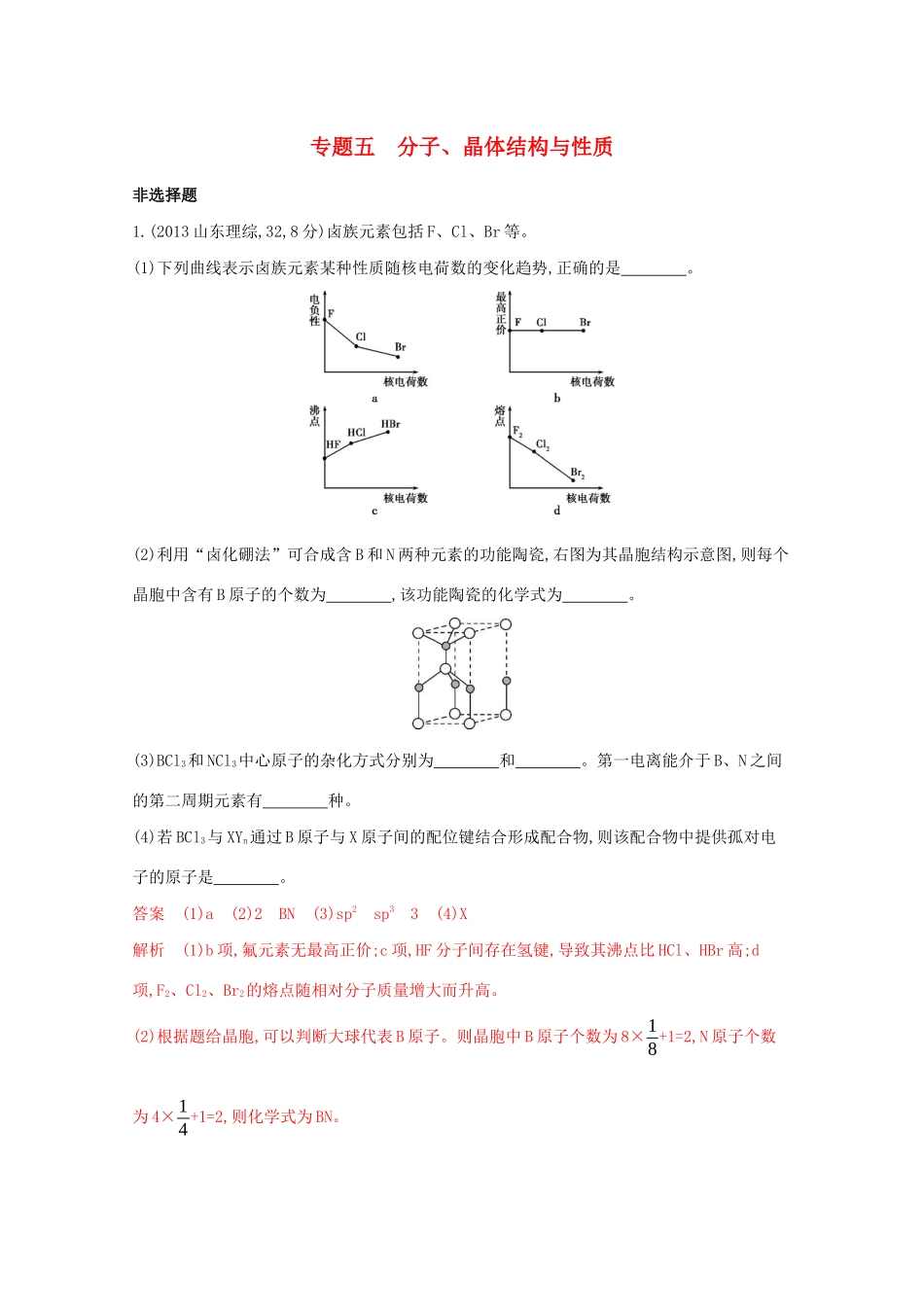
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,右图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为,该功能陶瓷的化学式为
(3)BCl3和NCl3中心原子的杂化方式分别为和
第一电离能介于B、N之间的第二周期元素有种
(4)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物中提供孤对电子的原子是
答案(1)a(2)2BN(3)sp2sp33(4)X解析(1)b项,氟元素无最高正价;c项,HF分子间存在氢键,导致其沸点比HCl、HBr高;d项,F2、Cl2、Br2的熔点随相对分子质量增大而升高
(2)根据题给晶胞,可以判断大球代表B原子
则晶胞中B原子个数为8×18+1=2,N原子个数为4×14+1=2,则化学式为BN
(3)判断第一电离能时要注意洪特规则,其中O原子第一电离能小于N原子但大于B原子,Be原子第一电离能大于B原子但小于N原子,故共有Be、C、O三种元素
(4)硼原子是缺电子体,故需要外界原子提供孤对电子
(2012山东理综,32,8分)金属镍在电池、合金、催化剂等方面应用广泛
(1)下列关于金属及金属键的说法正确的是
金属键具有方向性与饱和性b
金属键是金属阳离子与自由电子间的相互作用c
金属导电是因为在外加电场作用下产生自由电子d
金属具有光泽是因为金属阳离子吸收并放出可见光(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
CO与N2结构相似,CO分子内σ键与π键个数之比为
(4)甲醛(H2CO)在Ni催化作用下加氢可