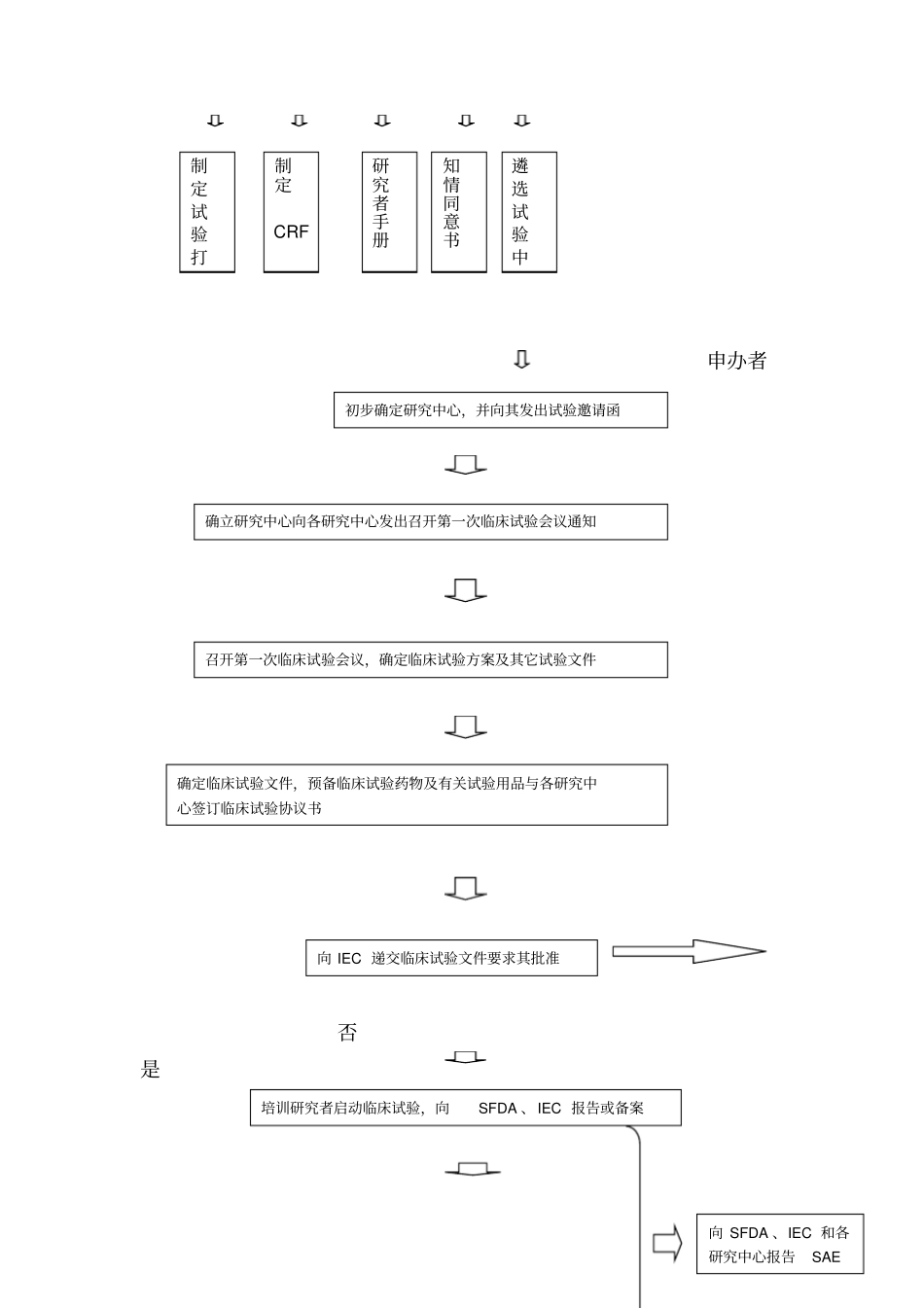
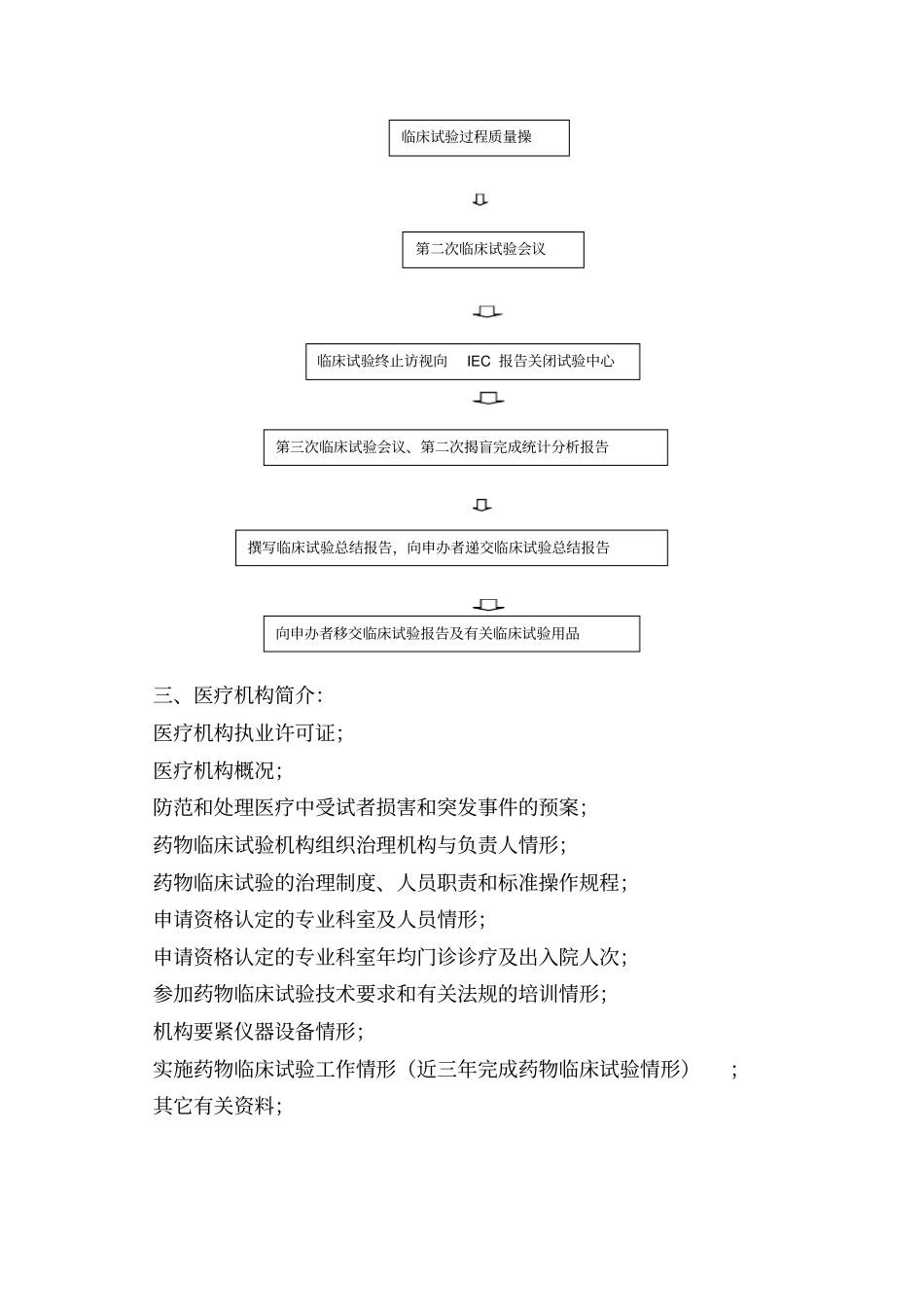
医院GCP认证标准文件一、国家药物临床试验机构组成图国家药物临床试验机构主任:副主任:国家药物临床试验机构办公室主任:秘书:运算机图文编辑:医学法律顾咨询:临床药理研究室:临床中心实验室:数据治理员:文件档案治理员:I期临床试验室:⋯⋯⋯⋯专业:⋯⋯⋯⋯专业:⋯⋯⋯⋯专业:二、国家药物临床试验机构作业流程申办者国家药物临床试验机构SFDA药物临床试验批文申办者申办者否是制定试验打制定CRF研究者手册知情同意书遴选试验中初步确定研究中心,并向其发出试验邀请函确立研究中心向各研究中心发出召开第一次临床试验会议通知召开第一次临床试验会议,确定临床试验方案及其它试验文件确定临床试验文件,预备临床试验药物及有关试验用品与各研究中心签订临床试验协议书向IEC递交临床试验文件要求其批准培训研究者启动临床试验,向SFDA、IEC报告或备案向SFDA、IEC和各研究中心报告SAE三、医疗机构简介:医疗机构执业许可证;医疗机构概况;防范和处理医疗中受试者损害和突发事件的预案;药物临床试验机构组织治理机构与负责人情形;药物临床试验的治理制度、人员职责和标准操作规程;申请资格认定的专业科室及人员情形;申请资格认定的专业科室年均门诊诊疗及出入院人次;参加药物临床试验技术要求和有关法规的培训情形;机构要紧仪器设备情形;实施药物临床试验工作情形(近三年完成药物临床试验情形);其它有关资料;临床试验过程质量操第二次临床试验会议临床试验终止访视向IEC报告关闭试验中心向申办者移交临床试验报告及有关临床试验用品第三次临床试验会议、第二次揭盲完成统计分析报告撰写临床试验总结报告,向申办者递交临床试验总结报告四、独立伦理委员会组成:独立伦理委员会主任:副主任:办公室秘书:独立伦理委员会成员:医学专家:非医学专家:医学法律顾咨询:社区/区行政人员:女性成员:五、独立医学伦理委员会成员履历表:六、独立医学伦理委员会审