第3节原子结构与元素的性质第2课时元素的电负性及其变化规律【教学目标】1
了解电负性的概念及内涵;2
认识主族元素电负性的变化规律并能给予解释
了解化合价与原子结构的关系
【教学重点】电负性概念及其变化规律
【教学难点】电负性变化规律【教学媒介】多媒体演示【教学方法】诱导——启发式、演绎推理和逻辑探究相结合教学【教学过程】教学环节活动时间教学内容教师活动学生活动设计意图一、复习旧课2分钟第一电离能的变化规律,并解释为什么N的第一电离能大于O的第一电离能学生回答问题复习强化上一节课的知识点二、联想·质疑3分钟电子亲和能第一电离能是原子失电子能力的定量描述,那么原子得电子能力的有如何用定量去描述呢
阅读电子亲和能引起学生知识的冲突,激发学习动机找出电子亲和能的变化规律学生讨论:没有规律研究电子亲和能没有太多的意义三、新课20分钟1
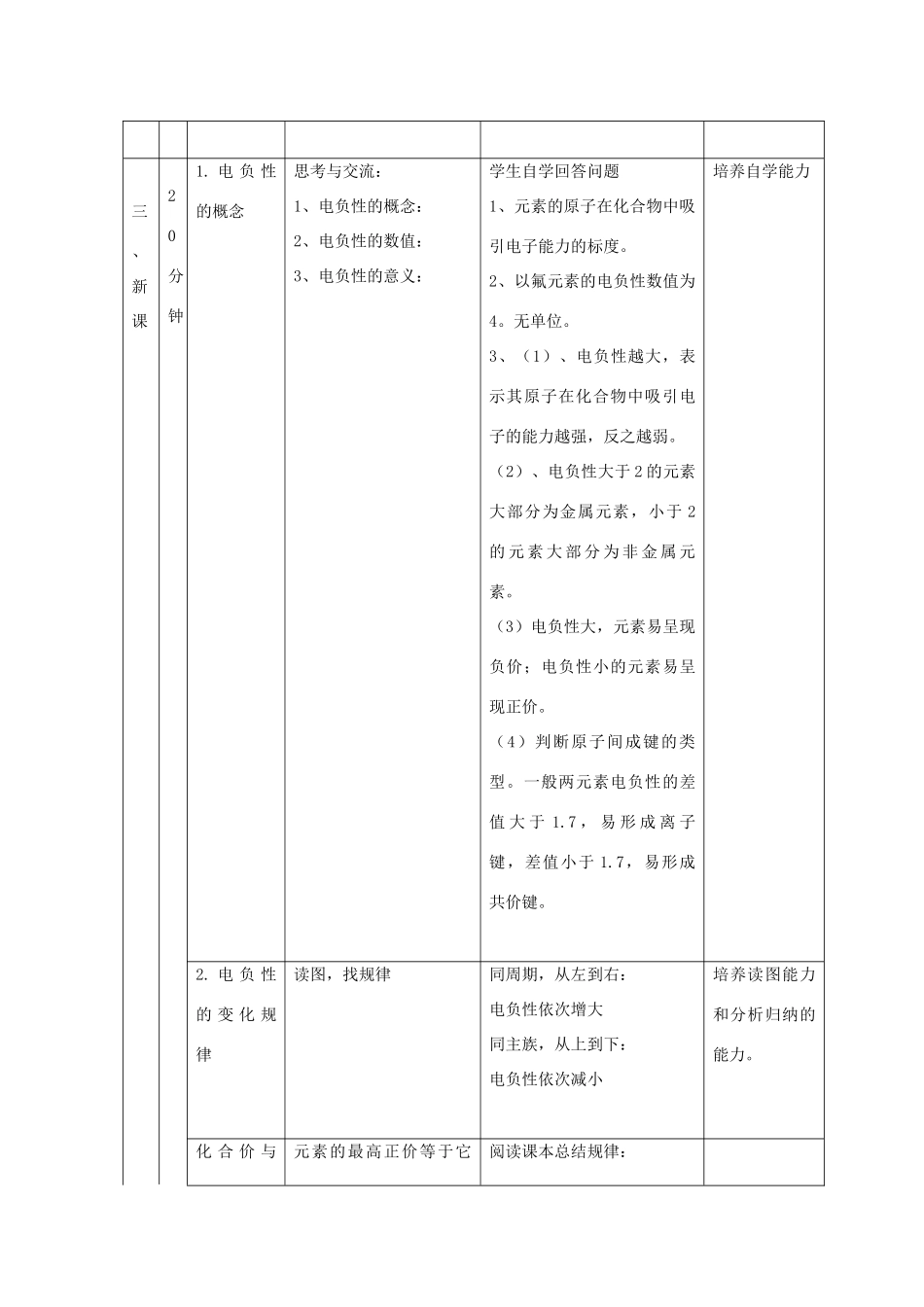
电负性的概念思考与交流:1、电负性的概念:2、电负性的数值:3、电负性的意义:学生自学回答问题1、元素的原子在化合物中吸引电子能力的标度
2、以氟元素的电负性数值为4
3、(1)、电负性越大,表示其原子在化合物中吸引电子的能力越强,反之越弱
(2)、电负性大于2的元素大部分为金属元素,小于2的元素大部分为非金属元素
(3)电负性大,元素易呈现负价;电负性小的元素易呈现正价
(4)判断原子间成键的类型
一般两元素电负性的差值大于1
7,易形成离子键,差值小于1
7,易形成共价键
培养自学能力2
电负性的变化规律读图,找规律同周期,从左到右:电负性依次增大同主族,从上到下:电负性依次减小培养读图能力和分析归纳的能力
化合价与元素的最高正价等于它阅读课本总结规律:电子排布的关系3
电负性的意义所在的族序数(除Ⅷ族和0族外)反映了原子间的成键能力和成键类型1
一般认为:电负性大于2
0的元素为非金属元素电负性小于2
0的元素为金属元素