化学键晶体结构诸城二中管延华考点聚焦1、理解离子键、共价键的含义
理解极性键和非极性键
了解极性分子和非极性分子
了解分子间作用力
初步了解氢键
2、了解几种晶体类型(离子晶体、原子晶体、分子晶体、金属晶体)及其性质
知识梳理物质结构的理论是高考的热点之一
要求理解原子的组成和结构,同位素,化学键,键的极性,晶体的类型和性质等
考查主要集中在8电子结构判断,电子式的书写,微粒半径的比较,晶体熔沸点高低判断,化学式的推导及有关晶体模型的计算等,在体现基础知识再现的同时,侧重观察、分析、推理能力的考查
近年来,往往从学科前沿或社会热点立意命题,引导学生关注科技发展,关注社会热点
化学键、离子键的概念化学键定义晶体或分子内直接相邻的两个或多个原子之间的强烈相互作用,通常叫做化学键
强烈的体现形式使原子间形成一个整体,彼此不能发生相对移动,只能在一定平衡位置振动
破坏这种作用需消耗较大能量
离子键定义阴、阳离子间通过静电作用所形成的化学键叫做离子键
本质阴阳离子间的静电作用形成条件和原因稳定的阳离子活泼金属MMn+活泼非金属Xm-离子键稳定的阴离子形成过程表示方法mM+nX→影响强度的因素及对物质性质的影响1
离子半径:离子半径越小,作用越强
含有该键的离子化合物的熔沸点就越高
离子电荷:离子电荷越多,作用越强
含有该键的离子化合物的熔沸点就越高
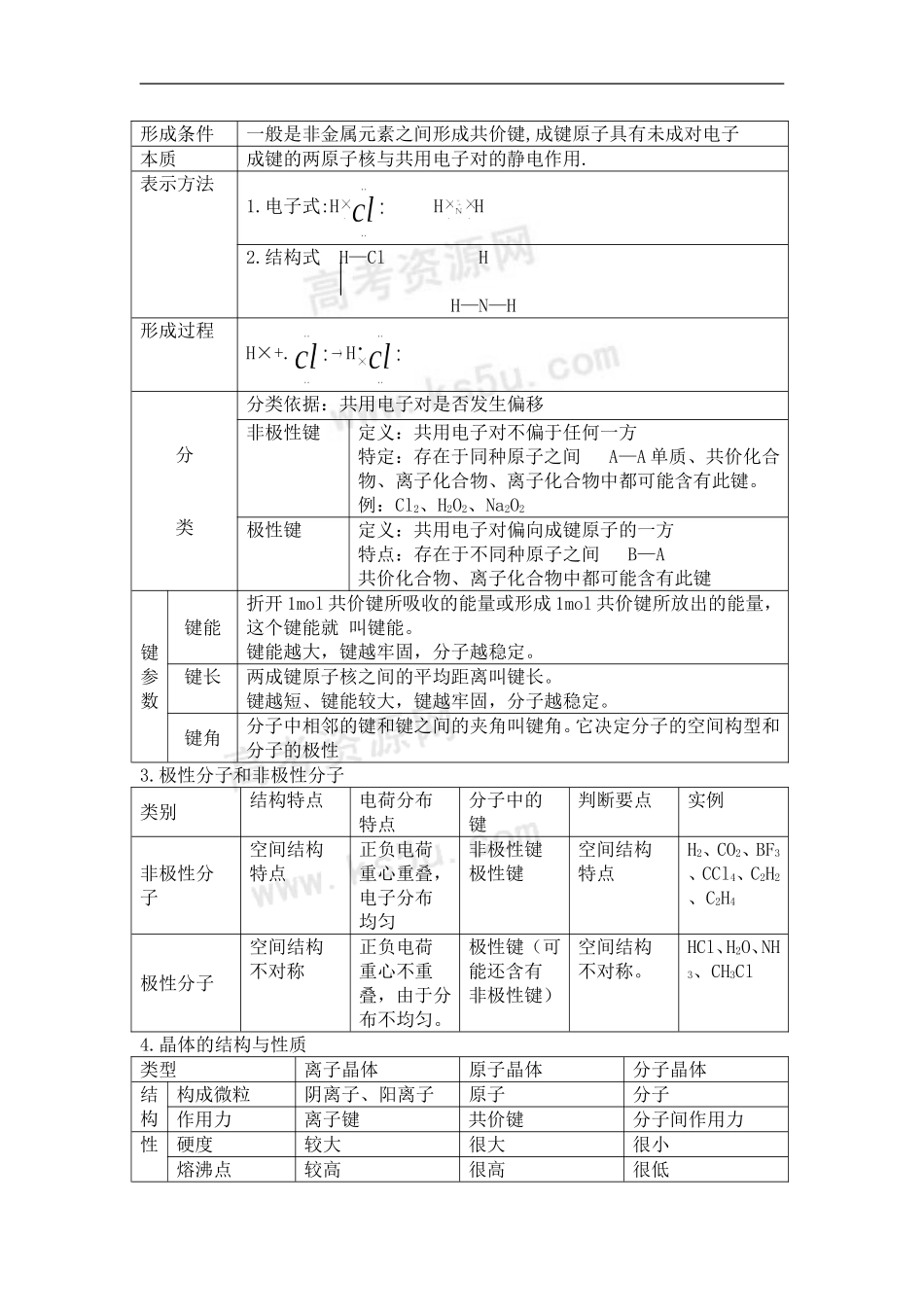
共价键定义原子间通过共用电子对所形成的化学键,叫共价键形成条件一般是非金属元素之间形成共价键,成键原子具有未成对电子本质成键的两原子核与共用电子对的静电作用
电子式:HHH2
结构式H—ClHH—N—H形成过程H×+
H分类分类依据:共用电子对是否发生偏移非极性键定义:共用电子对不偏于任何一方特定:存在于同种原子之间A—A单质、共价化合物、离子化合物、离子化合物中都可能含有此键
例:Cl2、H2O2、Na2O2极性