第一章第一节元素周期表(核素)课题:第一章第一节元素周期表(核素)授课班级课时第四课时教学目的知识与技能1、掌握核素的概念与用途、原子结构与元素性质的关系
2、具有把元素的性质、元素周期表的位置与元素组成微粒的结构初步联系起来并在一定条件下相互转化的运用能力
3、通过对元素性质的递变规律与元素组成微粒结构的联系
从而认识事物变化过程中量变引起质变的规律性,接受辨证唯物主义观点的教育
过程与方法1、培养学生的抽象思维能力和逻辑思维能力;通过对元素原子结构、位置间的关系的推导,培养学生的分析和推理能力
2、通过对元素周期律和元素周期表的关系的认识,渗透运用辩证唯物主义观点分析现象和本质的关系
情感态度价值观培养学生的求实、严谨和创新的优良品质;提高学生的学习兴趣重点核素的概念难点元素性质与核素的关系以及与同素异形体的区别课型讲授:习题:复习:讨论:其他:集体备课教案个人备课教案一、原子结构质子原子核外电子构成原子的粒子及其性质粒子电子质子中子电性和电量1个电子带1个单位负电荷1个质子带1个单位正电荷不显电性质量/kg9
109×10-311
673×10-271
675×10-27原子核中子相对质量1/1836(电子1
0071.008二、从表格得出原子的质量主要取决于哪种微粒
质子和中子的质量原子的质量主要集中在原子核,质子和中子的相对质量都近似为1,如果忽略电子的质量,将核内所有质子和中子的相对质量取近似值相加起来,所得的数值叫做质量数
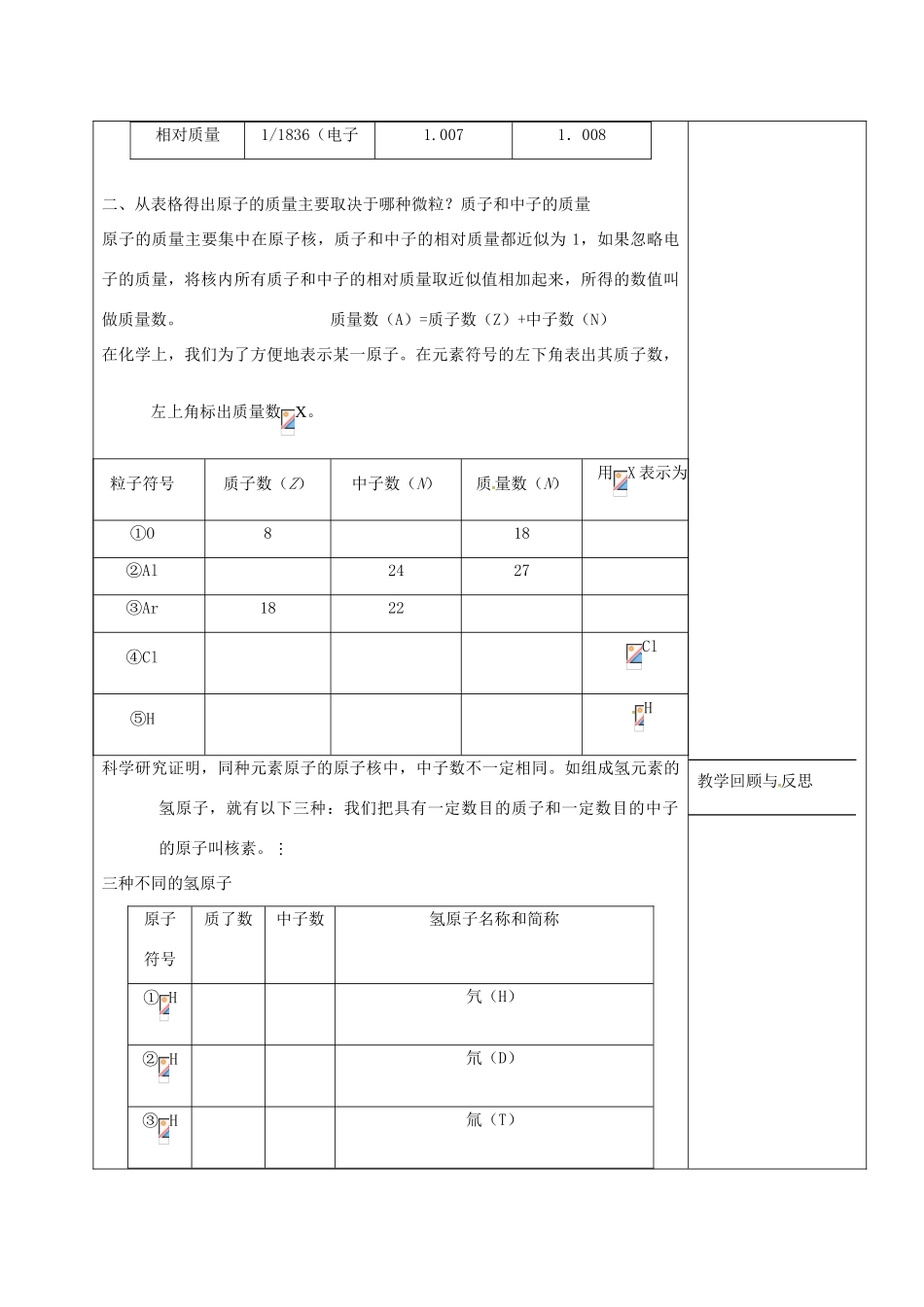
质量数(A)=质子数(Z)+中子数(N)在化学上,我们为了方便地表示某一原子
在元素符号的左下角表出其质子数,左上角标出质量数X
粒子符号质子数(Z)中子数(N)质量数(N)用X表示为①O818②Al2427③Ar1822④ClCl⑤HH科学研究证明,同种元素原子的原子核中,中子数不一定相同
如组成氢元素的氢原子,就有以下三种:我们把具有一