第1课时乙醇[核心素养发展目标]1
认识乙醇的组成及结构,知道乙醇的官能团是羟基,形成“结构决定性质”的观念,培养“宏观辨识与微观探析”的能力
认识乙醇的主要物理性质并掌握乙醇的主要化学性质,能从多角度动态地分析乙醇的化学变化,培养“变化观念”的学科素养
认识乙醇的官能团和性质间的关系,能根据乙醇结构对性质进行实验探究,培养“科学探究与创新意识”
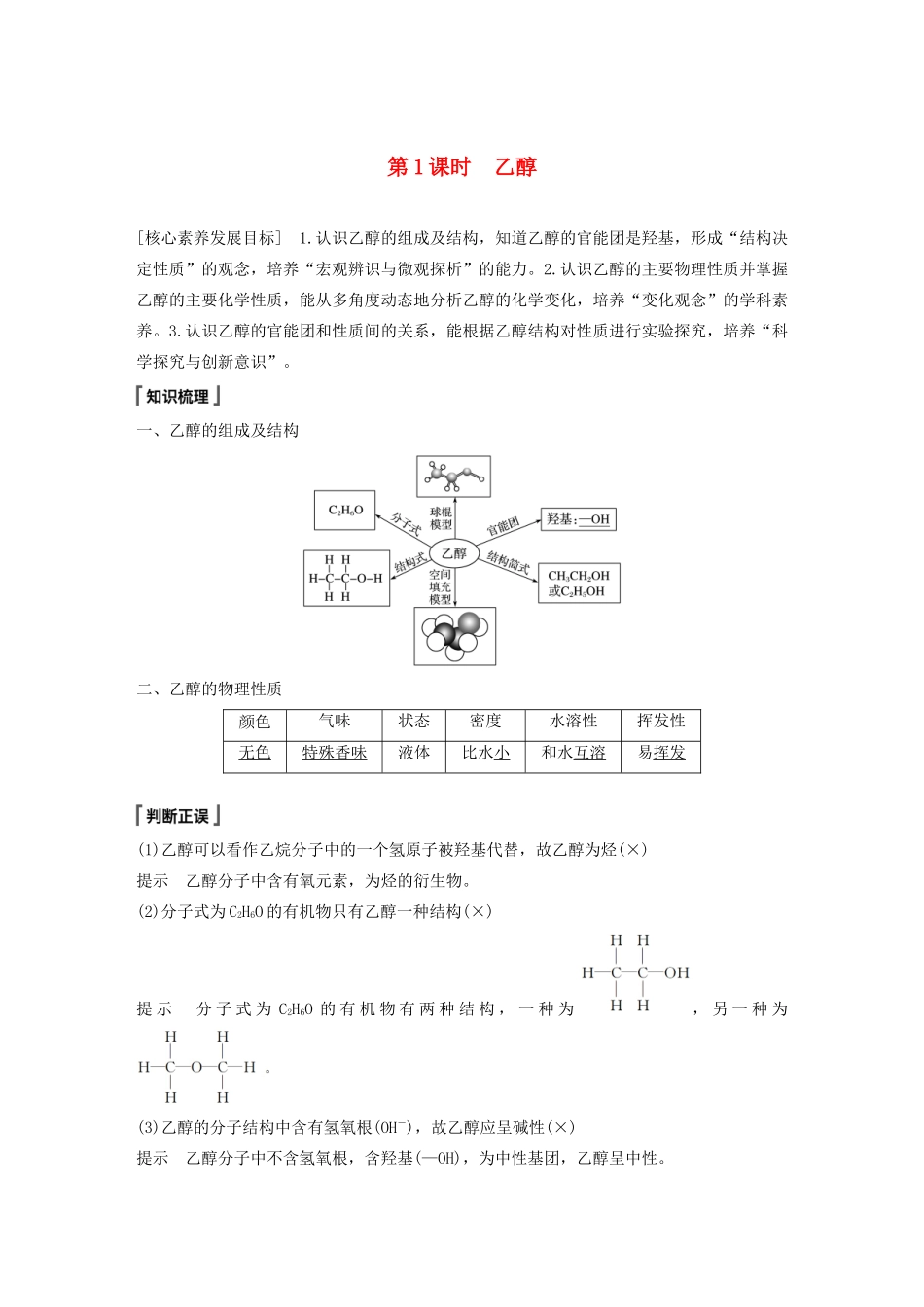
一、乙醇的组成及结构二、乙醇的物理性质颜色气味状态密度水溶性挥发性无色特殊香味液体比水小和水互溶易挥发(1)乙醇可以看作乙烷分子中的一个氢原子被羟基代替,故乙醇为烃(×)提示乙醇分子中含有氧元素,为烃的衍生物
(2)分子式为C2H6O的有机物只有乙醇一种结构(×)提示分子式为C2H6O的有机物有两种结构,一种为,另一种为(3)乙醇的分子结构中含有氢氧根(OH-),故乙醇应呈碱性(×)提示乙醇分子中不含氢氧根,含羟基(—OH),为中性基团,乙醇呈中性
(4)乙醇的官能团为—OH,决定了乙醇的化学性质(√)提示羟基(—OH)是乙醇的官能团,决定了乙醇的性质
(5)可以用分液的方法分离酒精和水的混合物(×)提示酒精和水互溶,无法用分液法分离,可用蒸馏法分离
(6)实验室常用无水CuSO4检验工业酒精中是否含水(√)提示无水CuSO4可以和水结合生成蓝色晶体,故可检验
(7)乙醇是优良的有机溶剂,可以萃取溴水中的溴(×)提示乙醇和水互溶,不能做萃取剂萃取溴水中的溴
(8)“美酒飘香”说明乙醇的沸点低(√)提示乙醇易挥发
三、乙醇的化学性质1.氧化反应(1)燃烧现象:乙醇在空气中燃烧,产生淡蓝色火焰,放出大量的热
化学方程式:C2H5OH+3O2――→2CO2+3H2O(2)催化氧化实验操作实验现象红色的铜丝――→变黑色――→变红色试管中的液体有刺激性气味实验原理2Cu+O2=====2CuO(铜丝变黑)――→CH3CHO+H2O+